м„ң лЎ
Nuclear protein in testis(NUT) midline carcinoma(NMC)лҠ” 15q14 м—јмғүмІҙм—җ мһҲлҠ” NUT мң м „мһҗмқҳ м—јмғүмІҙ мһ¬л°°м—ҙмқ„ нҠ№м§•мңјлЎң н•ҳлҠ”, л§Өмҡ° л“ңл¬јкі лҶ’мқҖ мӮ¬л§қлҘ мқ„ ліҙмқҙлҠ” нҺёнҸүм„ёнҸ¬м•”мў…мқҳ н•ң м•„нҳ•мқҙлӢӨ. ліөмһЎн•ң м—јмғүмІҙ мқҙмғҒ л°°м—ҙмқ„ ліҙмқҙлҠ” м „нҳ•м Ғмқё кі нҳ•м•”кіј лӢ¬лҰ¬ NMCлҠ” t(15;19) translocation лӢЁмқјмқҳ к°„лӢЁн•ң н•өнҳ•мқ„ ліҙмқҙлҠ” мғҲлЎңмҡҙ нҳ•нғңмқҳ м•”мў…мқҙлӢӨ[1]. NUT мң м „мһҗлҠ” м •мғҒмқём—җм„ң кі нҷҳ мЎ°м§Ғм—җм„ңл§Ң л°ңнҳ„лҗҳлҠ” кІғмңјлЎң нҷ•мқёлҗҳм—Ҳкі , к·ё кё°лҠҘмқҖ м•„м§Ғ л°қнҳҖм§Җм§Җ м•Ҡм•ҳлӢӨ. м•Ҫ 2/3м—җм„ң 19p13.1 м—јмғүмІҙм—җ мһҲлҠ” BRD4 мң м „мһҗк°Җ NUT мң м „мһҗмҷҖ translocationн•ҳм—¬ BRD4-NUT fusion oncogeneмқ„ нҳ•м„ұн•ҳкі , лӮҳлЁём§Җ 1/3м—җм„ңлҠ” BRD3 л“ұ лӢӨлҘё мң м „мһҗлҸ„ м•Ңл Өм ё мһҲлӢӨ[2]. BRD4лҠ” G2м—җм„ң MмңјлЎңмқҳ м„ёнҸ¬ мЈјкё°лҘј мЎ°м Ҳн•ЁмңјлЎңмҚЁ м„ёнҸ¬ мҰқмӢқм—җ мӨ‘мҡ”н•ң м—ӯн• мқ„ н•ҳлҠ” кІғмңјлЎң л°қнҳҖмЎҢлӢӨ. NMCм—җм„ң мқҙлҹ¬н•ң BRD4мқҳ кіјл°ңнҳ„мқҖ G1м—җм„ң SлЎңмқҳ 진н–үмқ„ м–өм ңн•ҳкІҢ лҗңлӢӨ. BRD4-NUT fusion oncogeneмқҖ мғҒн”јм„ёнҸ¬мқҳ м „кө¬мІҙм—җм„ң м•…м„ұ ліҖнҷ”лҘј мқјмңјнӮӨкі , лҸҷмӢңм—җ нҺёнҸүм„ёнҸ¬ 분нҷ”лҘј л§үм•„ м Җ분нҷ” лҳҗлҠ” лҜёл¶„нҷ” м•…м„ұ мў…м–‘мқҳ м„ұмһҘмқ„ мң лҸ„н•ңлӢӨкі м•Ңл Өм ё мһҲлӢӨ[2].
1991л…„м—җ 22м„ёмқҳ м—¬м„ұм—җм„ң мІҳмқҢмңјлЎң мқҙ мғҲлЎңмҡҙ нҳ•нғңмқҳ лҜёл¶„нҷ”м•”мў…мқҙ нқүм„ м—җм„ң л°ңкІ¬лҗҳм—ҲлӢӨ. t(15;19)(q14;p13.1) translocationмқҙ нҷ•мқёлҗҳм—Ҳкі , мқҙлҠ” BRD4-NUT лӢЁл°ұмқ„ л§Ңл“ңлҠ” oncogeneмңјлЎң л°қнҳҖмЎҢлӢӨ. мқҙлҹ¬н•ң м „мң„к°Җ мһҲлҠ” мў…м–‘л“Өмқҙ мЈјлЎң 비л¶Җ비лҸҷмқ„ нҸ¬н•Ён•ҳм—¬ лӘё мӨ‘м•ҷм„ мЈјліҖ кё°кҙҖм—җм„ң мғқкІЁ NUT midline carcinomaлқјкі лӘ…лӘ…лҗҳм—ҲлӢӨ[3]. к°ҖмһҘ нқ”нһҲ мғҒл¶Җкё°лҸ„мҶҢнҷ”кё°кҙҖ(50%)кіј мў…кІ©лҸҷ(41%)м—җм„ң л°ңмғқн•ҳл©°, к·ё мҷём—җ мқҙн•ҳм„ , м·ҢмһҘ, л¶ҖмӢ , н”јн•ҳ, м•Ҳкө¬, нҸҗ, л°©кҙ‘ к·ёлҰ¬кі мһҘкіЁ л“ұм—җм„ңлҸ„ ліҙкі лҗҳм—ҲлӢӨ[1].
NMCлҠ” лі‘лҰ¬ мҶҢкІ¬л§ҢмңјлЎңлҠ” 진лӢЁмқҙ м–ҙл ӨмӣҢ нҷ•м§„мқҙ лҠҰм–ҙм§Җкұ°лӮҳ м•Ҳ лҗҳлҠ” кІҪмҡ°к°Җ л§Һм•„ м•„м§Ғ л°ңлі‘лҘ мқҙ л¶ҲлӘ…нҷ•н•ҳлӢӨ. л‘җкІҪл¶Җ мҳҒм—ӯм—җм„ң л°ңмғқн•ҳлҠ” лҜёл¶„нҷ”м•”мў…мқҳ 18% м •лҸ„к°Җ NMCмқё кІғмңјлЎң мөңк·ј л…јл¬ёл“Өм—җм„ң ліҙкі лҗҳм—ҲлӢӨ[4,5]. мІҳмқҢ ліҙкі лҗң мҰқлЎҖм—җм„ңлҠ” NMCк°Җ мҶҢм•„лӮҳ м ҠмқҖ м„ұмқём—җ көӯн•ңлҗҳлҠ” кІғмІҳлҹј ліҙмҳҖмңјлӮҳ, мөңк·јм—җлҠ” лӮҳмқҙл“ м„ұмқём—җм„ңлҸ„ ліҙкі лҗҳкі мһҲлӢӨ[6].
NMCлҠ” reverse transcriptase-polymerase chain reaction(RT-PCR), fluorescence in situ hybridization(FISH), cytogenetic analysisлЎң NUT мң м „мһҗмқҳ мһ¬л°°м—ҙмқ„ нҷ•мқён•ЁмңјлЎңмҚЁ 진лӢЁмқҙ к°ҖлҠҘн•ҳлӢӨ[1]. н•ҳм§Җл§Ң мқҙлҹ¬н•ң кІҖмӮ¬л“ӨмқҖ мқјл°ҳм Ғмқё м•…м„ұ мў…м–‘м—җм„ңмқҳ кё°ліё кІҖмӮ¬м—җ н•ҙлӢ№н•ҳм§Җ м•Ҡкі , 비мҡ©м Ғ л¬ём ңк°Җ мһҲм—ҲмңјлӮҳ мөңк·ј NUT н•ӯмӣҗм—җ лҢҖн•ң мғҲлЎңмҡҙ лӢЁнҒҙлЎ м„ұн•ӯмІҙк°Җ к°ңл°ң лҗҳл©ҙм„ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷм—јмғүмқ„ нҶөн•ң 진лӢЁмқҙ 87%мқҳ лҜјк°җлҸ„мҷҖ 100%мқҳ нҠ№мқҙлҸ„лҘј ліҙм—¬мӨҢмңјлЎңмҚЁ мўӢмқҖ лҢҖмІҙм ңлЎң мӮ¬мҡ©лҗҳкі мһҲлӢӨ[7].
м•„м§Ғк№Ңм§ҖлҠ” NMCмқҳ м№ҳлЈҢк°Җ м •лҰҪлҗҳм–ҙ мһҲм§Җ м•ҠлӢӨ. NMCлҠ” л§Өмҡ° л№ лҘҙкІҢ мЈјліҖмңјлЎң м№ЁлІ”н•ҳкі мқҙлҘё мӢңкё°м—җ нҳҲн–үм„ұ м „нҢҢлҘјн•ҳм—¬ мӣҗкІ© м „мқҙк°Җ нқ”н•ҳлӢӨ. л•Ңл¬ём—җ лӢӨм•Ҫм ңн•ӯм•”м№ҳлЈҢ, л°©мӮ¬м„ м№ҳлЈҢ, мҲҳмҲ м Ғ м№ҳлЈҢ л“ұ лӢӨм–‘н•ң мЎ°н•©мқҳ м№ҳлЈҢлҘј н–Ҳм§Җл§Ң м№ҳлЈҢ кІ°кіјлҠ” л§ҢмЎұмҠӨлҹҪм§Җ м•Ҡм•ҳкі , нҷҳмһҗл“Өмқҳ нҸүк· мғқмЎҙ кё°к°„мқҖ 6.7к°ңмӣ”мқҙм—ҲлӢӨ[6]. кё°мЎҙмқҳ м№ҳлЈҢлЎңмҚЁлҠ” м•„м§Ғ к·јм№ҳм Ғ м№ҳлЈҢк°Җ м–ҙл ӨмӣҢ мғҲлЎңмҡҙ м№ҳлЈҢм—җ лҢҖн•ң м—°кө¬к°Җ 진н–ү мӨ‘мқҙлӢӨ. BRD4-NUT oncoproteinмқҙ histone acetylationмқ„ л§үм•„ м„ёнҸ¬ 분нҷ”лҘј л°©н•ҙн•ҳлҠ” мӮ¬мӢӨм—җ к·јкұ°н•ҳм—¬ histone deactylase inhibitorмҷҖ bromodomain in hibitorмқҳ мһ„мғҒм Ғ мӮ¬мҡ©мқҙ м—°кө¬ мӨ‘мқҙлӢӨ[2].
нҳ„мһ¬ көӯлӮҙм—җм„ңлҠ” Park л“ұ[8]мқҙ ліҙкі н•ң мқҙн•ҳм„ м—җм„ң л°ңмғқн•ң NMC ліҙкі к°Җ мң мқјн•ҳлӢӨ. NMCмқҳ мЈј л°ңлі‘ кё°кҙҖмңјлЎң 비л¶Җ비лҸҷ мҳҒм—ӯмқҙ нқ”нһҲ ліҙкі лҗҳкі мһҲм–ҙ мқҙ비мқёнӣ„кіјмқҳ м—ӯн• мқҙ мӨ‘мҡ”н•ҳлӢӨкі н• мҲҳ мһҲлӢӨ. мқҙм—җ ліё м Җмһҗл“ӨмқҖ 9к°ңмӣ” лҸҷм•Ҳ н•ң кё°кҙҖм—җм„ң л°ңмғқн•ң 비л¶Җ비лҸҷ мҳҒм—ӯмқҳ NMC л‘җ мҰқлЎҖлҘј ліҙкі н•ҳкі мһҗ н•ңлӢӨ.
мҰқ лЎҖ
м„ңмҡёлҢҖн•ҷкөҗлі‘мӣҗм—җм„ңлҠ” NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬к°Җ 2015л…„ 10мӣ”л¶Җн„° мӢңмһ‘лҗҳм—ҲлӢӨ. 2015л…„ 10мӣ” 1мқјл¶Җн„° 2015л…„ 6мӣ” 30мқјк№Ңм§Җ мҙқ 9к°ңмӣ” лҸҷм•Ҳ ліёмӣҗм—җм„ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬мғҒ NMCлЎң 진лӢЁмқ„ л°ӣмқҖ нҷҳмһҗлҠ” мҙқ 4лӘ…мқҙм—ҲлӢӨ. 4лӘ…мқҳ нҷҳмһҗ мӨ‘ 2лӘ…мқҖ нҸҗм•”мңјлЎң ліё л…јл¬ём—җм„ңлҠ” м ңмҷён•ҳмҳҖкі , 비л¶Җ비лҸҷ кё°мӣҗмқё лӮҳлЁём§Җ 2лӘ…мқҳ мқҳл¬ҙ кё°лЎқмқ„ кІҖнҶ н•ҳмҳҖлӢӨ.
мҰқ лЎҖ 1
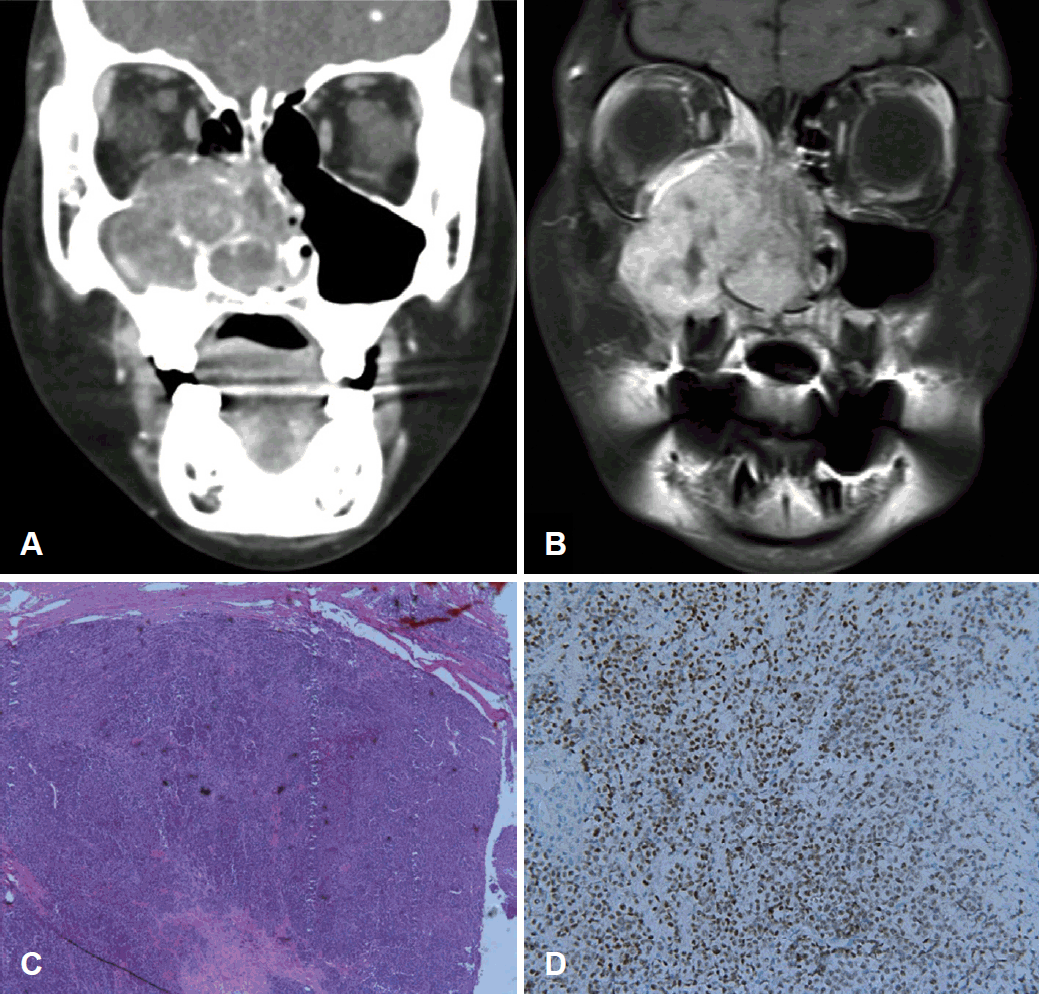
8м„ё лӮЁмһҗк°Җ мҡ°мёЎ мҪ”л§үнһҳмқ„ мЈјмҶҢлЎң мқҙ비мқёнӣ„кіј мҷёлһҳлЎң лӮҙмӣҗн•ҳмҳҖлӢӨ. кІҖ진мғҒ мҡ°мёЎ 비강мқ„ мұ„мҡ°лҠ” кіјнҳҲкҙҖм„ұ мў…кҙҙ мҶҢкІ¬мқ„ нҷ•мқён• мҲҳ мһҲм—ҲлӢӨ. мқҙм—җ CTмҷҖ MRIлҘј мӢңн–үн•ҳмҳҖкі 4.5 cm нҒ¬кё°мқҳ мҡ°мёЎ мғҒм•…лҸҷмқ„ мӨ‘мӢ¬мңјлЎң мЎ°мҳҒ мҰқк°•мқ„ ліҙмқҙлҠ” мў…кҙҙлҘј кҙҖм°°н• мҲҳ мһҲм—ҲлӢӨ. мқҙлҠ” мҡ°мёЎ 비강, мёЎл‘җкіЁн•ҳ кіөк°„мқ„ м№ЁлІ”н•ҳкі мҡ°мёЎ м•Ҳкө¬лҘј лҲ„лҘҙлҠ” м–‘мғҒмқ„ ліҙмҳҖлӢӨ. лҳҗн•ң мҡ°мёЎ мғҒм•…лҸҷмқҳ мғҒ, нӣ„, лӮҙмёЎлІҪ л°Ҹ 비мӨ‘кІ©мқ„ нҢҢкҙҙн•ҳлҠ” мҶҢкІ¬мқҙ мһҲм—ҲлӢӨ(Fig. 1A and B). лӮҙмӢңкІҪн•ҳ мЎ°м§ҒкІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі лҜёл¶„нҷ”м•”мў…мңјлЎң 진лӢЁлҗҳм–ҙ (Fig. 1C) positron emission tomography(PET) кІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі мӣҗкІ© м „мқҙлҘј мӢңмӮ¬н•ҳлҠ” мҶҢкІ¬мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ. мқҙнӣ„ cisplatin, bleomycin, 5-fluorouracil н•ӯм•”нҷ”н•ҷм№ҳлЈҢлҘј мӢңмһ‘н•ҳмҳҖлӢӨ. мӨ‘к°„м—җ 5-fluorouracil кҙҖл Ё лҮҢлі‘мҰқ л°ңмғқмңјлЎң epirubicinмңјлЎң ліҖкІҪн•ҳмҳҖлӢӨ. н•ӯм•”нҷ”н•ҷм№ҳлЈҢм—җ л°ҳмқ‘мқҙ нҒ¬м§Җ м•Ҡм•„ м•Ҳкө¬лҘј ліҙмЎҙн•ҳлҠ” мғҒм•…м Ҳм ңмҲ мқ„ мӢңн–үн•ҳмҳҖкі н•ҙлӢ№ мЎ°м§Ғм—җм„ң л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј нҷ•мқён•ҙ ліё кІ°кіј NUT(Fig. 1D), cytokeratin, epithelial membrane antigen vimentin, FLI-1, P40м—җ м–‘м„ұ л°ҳмқ‘мқ„ ліҙм—¬ NMCлЎң нҷ•м§„лҗҳм—ҲлӢӨ. мҲҳмҲ нӣ„ docetaxel, ifosfamide, cisplatin н•ӯм•”м№ҳлЈҢмҷҖ мҡ°мёЎ мғҒм•…м—җ 54 GyлҘј 30нҡҢ л¶„н• н•ҳм—¬ л°©мӮ¬м„ м№ҳлЈҢлҘј 진н–үн•ҳкі мһҲлӢӨ. мІҳмқҢ лҜёл¶„нҷ”м•”мў…мңјлЎң 진лӢЁл°ӣмқҖ мқҙлһҳлЎң л§Ҳм§Җл§ү мҷёлһҳ л°©л¬ёк№Ңм§Җмқё 9к°ңмӣ”к°„ мғқмЎҙ мӨ‘мқҙлӢӨ(Table 1).
мҰқ лЎҖ 2
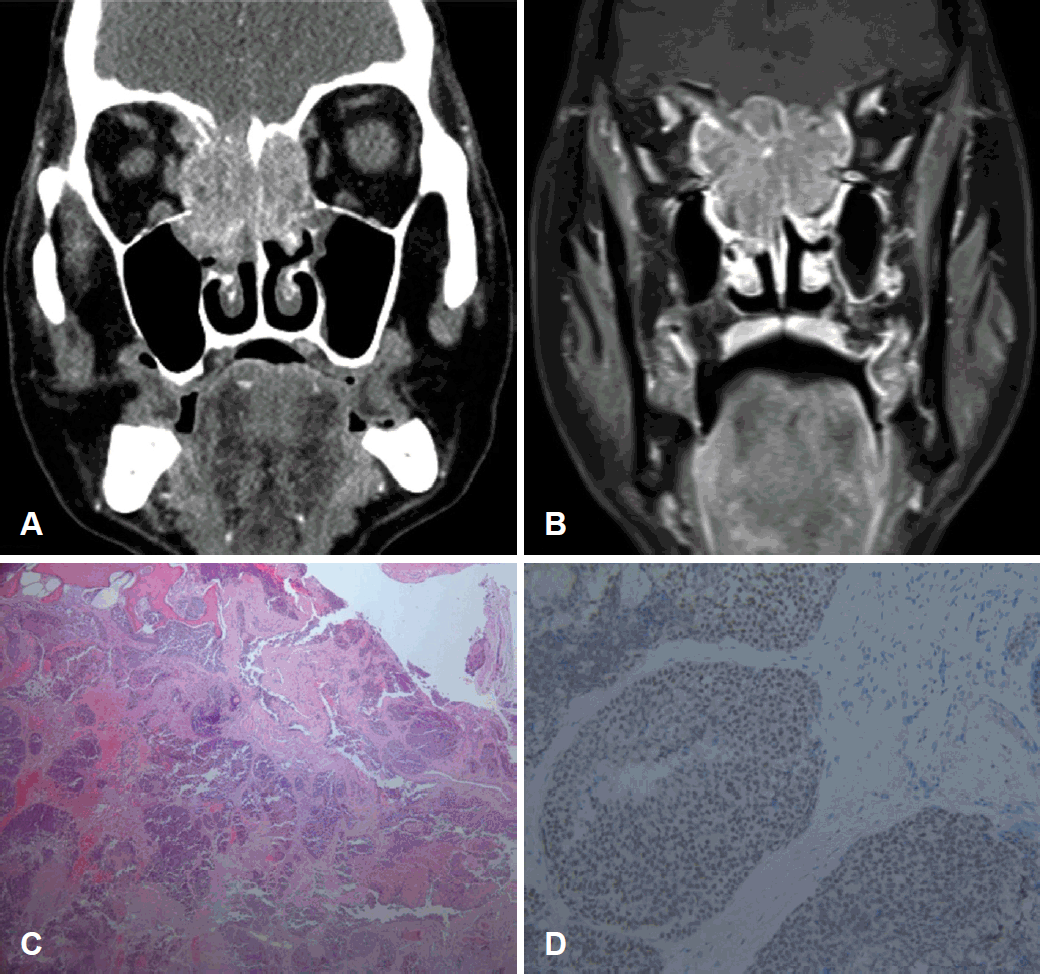
65м„ё лӮЁмһҗк°Җ л‘җнҶө, мҡ°мёЎ м•Ҳкө¬ л¶Җмў…, мҡ°мёЎ мӢңл Ҙ м Җн•ҳлҘј мЈјмҶҢлЎң ліёмӣҗ мқ‘кёүмӢӨлЎң лӮҙмӣҗн•ҳмҳҖлӢӨ. кІҖ진мғҒ м–‘мёЎ мӨ‘비갑к°ң мӮ¬мқҙм—җ мў…кҙҙ мҶҢкІ¬мқ„ нҷ•мқён• мҲҳ мһҲм—ҲлӢӨ. мқҙм—җ MRIмҷҖ CTлҘј мӢңн–үн•ҳмҳҖкі 4.5 cm нҒ¬кё°мқҳ мҡ°мёЎ мӮ¬кіЁлҸҷмқ„ мӨ‘мӢ¬мңјлЎң мЎ°мҳҒ мҰқк°•мқ„ ліҙмқҙлҠ” мў…кҙҙлҘј кҙҖм°°н• мҲҳ мһҲм—ҲлӢӨ. мқҙлҠ” м–‘мёЎ мӮ¬кіЁлҸҷ, м–‘мёЎ 비강, м–‘мёЎ м ‘нҳ•лҸҷ, м „л‘җк°ңм ҖлҘј м№ЁлІ”н•ҳкі м–‘мёЎ м•Ҳкө¬лҘј лҲ„лҘҙлҠ” м–‘мғҒмқ„ ліҙмҳҖлӢӨ(Fig. 2A and B). PET кІҖмӮ¬мғҒ мӣҗкІ© м „мқҙлҘј мӢңмӮ¬н•ҳлҠ” мҶҢкІ¬мқҖ кҙҖм°°лҗҳм§Җ м•Ҡм•ҳлӢӨ. лӮҙмӢңкІҪн•ҳ нҺҖм№ҳмғқкІҖмқ„ мӢңн–үн•ҳмҳҖкі м Җ분нҷ”м•”мў…мңјлЎң 진лӢЁлҗҳм—ҲлӢӨ(Fig. 2C). мқҙм—җ 추к°ҖлЎң л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј мӢңн–үн•ҳмҳҖкі NUT(Fig. 2D), cytokeratin, P40м—җ м–‘м„ұ л°ҳмқ‘мқ„ ліҙм—¬ NMCлЎң нҷ•м§„лҗҳм—ҲлӢӨ. нҷҳмһҗлҠ” лӮҙмӢңкІҪн•ҳл‘җк°ңм•Ҳл©ҙм Ҳм ңмҲ л°Ҹ мӢңмӢ кІҪк°җм••мҲ мқ„ мӢңн–үл°ӣм•ҳкі мҲҳмҲ нӣ„ 67.5GyлҘј 30нҡҢ л¶„н• н•ң л°©мӮ¬м„ м№ҳлЈҢмҷҖ н•Ёк»ҳ cisplatinмқ„ 6мЈјк°„ мӮ¬мҡ©н•ҳлҠ” лҸҷмӢңн•ӯм•”нҷ”н•ҷл°©мӮ¬м„ м№ҳлЈҢлҘј л°ӣм•ҳлӢӨ. мқҙнӣ„ кІҪкіј кҙҖм°°мӨ‘мңјлЎң нҺҖм№ҳмғқкІҖмңјлЎң нҷ•м§„мқ„ л°ӣмқҖ мқҙлһҳлЎң л§Ҳм§Җл§ү мҷёлһҳ л°©л¬ёк№Ңм§Җмқё 5к°ңмӣ”к°„ мғқмЎҙ мӨ‘мқҙлӢӨ.
кі м°°
ліё мҰқлЎҖл“Өмқҳ м—°л №мқҖ 8м„ёмҷҖ 65м„ёмҳҖкі лӘЁл‘җ лӮЁмһҗмқҙл©° 비нқЎм—°мһҗмҳҖлӢӨ. мІҳмқҢм—җлҠ” NMCк°Җ мҶҢм•„ лҳҗлҠ” м ҠмқҖ м„ұмқём—җм„ң л°ңмғқн•ңлӢӨкі ліҙкі н•ҳмҳҖмңјлӮҳ мқҙлҠ” м„ёнҸ¬мң м „н•ҷм Ғ кІҖмӮ¬к°Җ м„ұмқёліҙлӢӨлҠ” мЈјлЎң мҶҢм•„мқҳ м•…м„ұ мў…м–‘м—җм„ң мһҗмЈј мӢңн–үлҗҳкё° л•Ңл¬ём—җ л°ңмғқн•ҳлҠ” н‘ңліём„ м • нҺёнҢҢлЎң мғқк°Ғлҗҳкі мһҲлӢӨ[5]. 78м„ё нҷҳмһҗ л“ұ лӮҳмқҙл“ м„ұмқёкө°м—җм„ңлҸ„ NMCк°Җ 진лӢЁлҗҳм–ҙ лӘЁл“ м—°л №кө°м—җм„ң кі л Өлҗҳм–ҙм•ј н•Ёмқ„ ліҙкі н•ҳмҳҖлӢӨ[5]. Bishopкіј Westra[4]лҠ” 151лӘ…мқҳ 비л¶Җ비лҸҷм•” нҷҳмһҗ мӨ‘ 2%к°Җ NMCмһ„мқ„ ліҙкі н•ҳмҳҖкі к·ёл“Өмқҳ нҸүк· м—°л №мқҖ 36м„ёмҳҖкі лӘЁл‘җ лӮЁмһҗмқҙл©° 2лӘ…мқҖ 비нқЎм—°мһҗмҳҖкі 1лӘ…мқҖ кіјкұ° нқЎм—°л Ҙмқҙ мһҲлҚҳ нҷҳмһҗмҳҖлӢӨ. мқјл°ҳм ҒмңјлЎң нқЎм—°л Ҙмқҙ мһҲлҠ” нҷҳмһҗм—җм„ң 비л¶Җ비лҸҷм•”мқҙ нқ”н•ҳлӮҳ 비л¶Җ비лҸҷм—җм„ңмқҳ NMCлҠ” 비нқЎм—°мһҗм—җм„ң лҚ” нқ”н–ҲлӢӨ[7]. к·ёлҹ¬лӮҳ нҷҳмһҗ мҲҳк°Җ л§Һм§Җ м•Ҡм•„ л°ңмғқн•ҳлҠ” мҳӨлҘҳмқј к°ҖлҠҘм„ұлҸ„ л°°м ңн• мҲҳ м—ҶлӢӨ.
NMCмқҳ 진лӢЁмқҖ ліё м Җмһҗл“Өмқҳ лі‘мӣҗм—җм„ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј нҶөн•ҙ 2015л…„ 10мӣ”л¶Җн„° мӢңмһ‘н•ҳмҳҖлӢӨ. мҳҲм „м—җлҠ” RTPCR, FISH лҳҗлҠ” cytogenetic analysis л“ұ мң м „мһҗ кІҖмӮ¬лҘј нҶөн•ҙм„ңл§Ң 진лӢЁмқҙ к°ҖлҠҘн–Ҳкё° л•Ңл¬ём—җ 비мҡ©м Ғ л¬ём ңк°Җ мһҲм—Ҳм§Җл§Ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬к°Җ к°ҖлҠҘн•ҙм§Җл©ҙм„ң нҠ№мқҙлҸ„ 100%, лҜјк°җлҸ„ 87%мқҳ 진лӢЁмқҙ к°ҖлҠҘн•ҙмЎҢлӢӨ. лӢӨл§Ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬мғҒ м–‘м„ұмҶҢкІ¬мқҖ NMCм—җл§Ң көӯн•ңлҗң кІғмқҖ м•„лӢҲкі мғқмӢқм„ёнҸ¬мў…м—җм„ңлҸ„ м–‘м„ұмқј мҲҳ мһҲлӢӨ. мғҒл¶Җкё°лҸ„мҶҢнҷ”кё°кҙҖкіј мў…кІ©лҸҷм—җ л°ңмғқн•ң лҜёл¶„нҷ”м•”м—җм„ң NMCлҝҗл§Ң м•„лӢҲлқј мғқмӢқм„ёнҸ¬мў…мқҳ м „мқҙ к°ҖлҠҘм„ұлҸ„ кі л Өн•ҙм•ј н•ңлӢӨ[7].
лі‘лҰ¬мЎ°м§ҒкІҖмӮ¬мғҒ 1лІҲ мҰқлЎҖлҠ” мІҳмқҢм—җ 비мқёл‘җ лҜёл¶„нҷ”м•”мў…мңјлЎң 진лӢЁлҗҳм—Ҳкі NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј мӢңн–үн•ҳм§Җ м•Ҡм•ҳлӢӨ. мқҙм—җ н•ӯм•”нҷ”н•ҷм№ҳлЈҢлҘј лЁјм Җ мӢңмһ‘н•ҳмҳҖкі мў…кҙҙмқҳ нҒ¬кё°к°Җ мӨ„м–ҙл“ңлҠ” м–‘мғҒмқ„ ліҙмҳҖмңјлӮҳ нҡЁкіјмқҳ н•ңкі„к°Җ мһҲм–ҙ мҲҳмҲ м Ғ м№ҳлЈҢлҘј кі„нҡҚн•ҳкІҢ лҗҳм—ҲлӢӨ. NMC к°ҖлҠҘм„ұмқ„ нҷ•мқён•ҳкё° мң„н•ҙ мҲҳмҲ нӣ„ мЎ°м§Ғм—җм„ң NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј н•Ёк»ҳ мӢңн–үн•ҳмҳҖкі мҲҳмҲ нӣ„м—җ NMCлЎң нҷ•м§„лҗҳм—ҲлӢӨ. 2лІҲ мҰқлЎҖлҠ” мІҳмқҢ нҺҖм№ҳмғқкІҖм—җм„ң 비л¶Җ비лҸҷ м Җ분нҷ”м•”мў…мңјлЎң 진лӢЁлҗҳм—Ҳкі NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј н•Ёк»ҳ мӢңн–үн•ҳмҳҖлӢӨ. к·ёлһҳм„ң 1лІҲ мҰқлЎҖм—җ 비н•ҙ мўҖ лҚ” л№ЁлҰ¬ NMCк°Җ нҷ•м§„лҗҳм—ҲлӢӨ.
ліё мҰқлЎҖм—җм„ң NUT мҷёмқҳ л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬ кІ°кіјлҠ” нҶөмқјлҗң кІҖмӮ¬лҘј мӢңн–үн•ҳм§Җ м•Ҡм•ҳм§Җл§Ң 1лІҲ мҰқлЎҖм—җм„ң chromogranin, S-100, synaptophysinм—җ мқҢм„ұ, 2лІҲ мҰқлЎҖм—җм„ң desmin, CD99, Epstein-Barr virus(EBV)м—җ мқҢм„ұ мҶҢкІ¬мқ„ ліҙмҳҖлӢӨ(Table 2). нҠ№м§•м ҒмңјлЎң NMCлҠ” лі‘лҰ¬мЎ°м§ҒкІҖмӮ¬мғҒ лҜёл¶„нҷ”м•”мў…мқ„ м ңмҷён•ҳкі лҠ” CD45, S-100, HMB-45, CD99, desmin, myoglobin, smooth muscle actin, muscle actin, neuron-specific enolase, CD57, chromogranin, synaptophysin, alpha-fetoprotein, placental alkaline phophatase л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬мғҒ мқҢм„ұмқ„ нҷ•мқён•ЁмңјлЎңмҚЁ лӢӨлҘё м•…м„ұ мў…м–‘кіј к°җлі„ 진лӢЁмқ„ н• мҲҳ мһҲлӢӨ. лҜёл¶„нҷ”м•”мў…кіјмқҳ к°җлі„ 진лӢЁмқ„ мң„н•ң л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬м—җм„ң 비мқёл‘җм•”мқҳ лҜёл¶„нҷ”нҳ•мқҳ кІҪмҡ° EBV кІҖмӮ¬мғҒ м–‘м„ұмқҙм§Җл§Ң NMCм—җм„ңлҠ” ліҙкі лҗң лӘЁл“ кІҪмҡ°м—җм„ң мқҢм„ұмқҙм—ҲлӢӨ. 비л¶Җ비лҸҷ лҜёл¶„нҷ”м•”мў…мқҳ кІҪмҡ° лҢҖл¶Җ분 p63мқҳ л°ҳмқ‘мқҙ м—ҶмңјлӮҳ NMCм—җм„ңлҠ” лҢҖл¶Җ분 p63мқҳ л©ҙм—ӯл°ҳмқ‘мқ„ нҷ•мқён• мҲҳ мһҲм—Ҳкі лҳҗн•ң CD34м—җ л°ҳмқ‘мқ„ ліҙмҳҖлӢӨ[9]. NMC 진лӢЁм—җ лҢҖн•ҙ Bauer л“ұ[6]мқҖ нқүк°• л°Ҹ л‘җкІҪл¶Җм—җ л°ңмғқн•ҳлҠ” мғҳ분нҷ”к°Җ м—ҶлҠ” лӘЁл“ м Җ분нҷ”м•”мў…м—җ лҢҖн•ҙ NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј н• кІғмқ„ 추мІңн–ҲлӢӨ. мғҒ피분нҷ” м—¬л¶ҖлҠ” кІҖмӮ¬мқҳ кІ°м •м—җ мҳҒн–Ҙмқ„ мЈјм§Җ м•Ҡм§Җл§Ң, EBV лҳҗлҠ” human papilloma virus к°җм—ј л“ұ нҠ№м •н•ң мӣҗмқёмқҙ лЁјм Җ нҷ•мқёлҗң кІҪмҡ°лҠ” кІҖмӮ¬лҘј н•„мҡ”лЎң н•ҳм§Җ м•ҠлҠ”лӢӨкі н•ҳмҳҖлӢӨ.
NMCмқҳ м№ҳлЈҢлҠ” м•„м§Ғ м •лҰҪлҗҳм§Җ м•Ҡм•ҳлӢӨ. мўҖ лҚ” л№ лҘё мӢңкё°м—җ л°©мӮ¬м„ м№ҳлЈҢлҘј мӢңмһ‘н• мҲҳлЎқ, мңЎм•Ҳм ҒмңјлЎң мў…м–‘м „м Ҳм ңк°Җ к°ҖлҠҘн–Ҳмқ„ л•Ң мғқмЎҙ кё°к°„мқҙ нҶөкі„н•ҷм ҒмңјлЎң мң мқҳлҜён•ҳкІҢ мҰқк°Җн•ҳмҳҖмңјлӮҳ, н•ӯм•”м№ҳлЈҢлҠ” нҡЁкіјлҘј мһ…мҰқн•ҳм§Җ лӘ»н–ҲлӢӨкі ліҙкі н–ҲлӢӨ[6]. Chau л“ұ[10]мқҖ 48лӘ…мқҳ л‘җкІҪл¶Җ мҳҒм—ӯм—җ л°ңмғқн•ң NMC нҷҳмһҗл“Өмқ„ кҙҖм°°н•ҳмҳҖкі мҙҲкё° м№ҳлЈҢлЎң кҙ‘лІ”мң„н•ң м Ҳм ңмҷҖ н•Ёк»ҳ м Ҳм ң кІҪкі„л©ҙм—җм„ң м•…м„ұм„ёнҸ¬к°Җ нҷ•мқёлҗҳм§Җ м•Ҡмқ„ л•Ң нҶөкі„н•ҷм ҒмңјлЎң мң мқҳлҜён•ҳкІҢ нҸүк· мғқмЎҙ кё°к°„ л°Ҹ л¬ҙ진н–ү мғқмЎҙ кё°к°„мқ„ н–ҘмғҒмӢңнӮЁлӢӨкі ліҙкі н–ҲлӢӨ. л°ҳл©ҙ мҙҲкё° м№ҳлЈҢлЎң л°©мӮ¬м„ м№ҳлЈҢ л°Ҹ н•ӯм•”нҷ”н•ҷм№ҳлЈҢлҠ” мғқмЎҙ кё°к°„м—җ мң мқҳлҜён•ң мҳҒн–Ҙмқ„ мЈјм§Җ лӘ»н–ҲмңјлӮҳ ліҙмЎ° м№ҳлЈҢлЎңмҚЁ мӨ‘мҡ”н•ң м—ӯн• мқ„ н•ңлӢӨкі н•ҳмҳҖлӢӨ.
NMCлҠ” мһ„мғҒмў…м–‘н•ҷмқҳ 분мһҗн•ҷм Ғ нҠ№м„ұмқҙ мӨ‘мҡ”н•ң нҢЁлҹ¬лӢӨмһ„ ліҖнҷ”мқҳ мўӢмқҖ мҳҲмқҙлӢӨ. н•ҙл¶Җн•ҷм Ғ кө¬мЎ°к°Җ м•„лӢҲлқј кіөнҶөлҗң мң м „лі‘лҰ¬мғқлҰ¬н•ҷм Ғ нҠ№м„ұмңјлЎң нҶөн•©лҗң м§Ҳнҷҳмқҙкё° л•Ңл¬ёмқҙлӢӨ. мөңк·ј мғқл¬јн•ҷм Ғ м—°кө¬мқҳ 진ліҙмҷҖ н•Ёк»ҳ NMCм—җм„ң bromodomain-containing NUT fusion proteinмқҙ histone acetylationмқ„ л°©н•ҙн•ҳм—¬ м„ёнҸ¬мқҳ 분нҷ”лҘј л§үлҠ” кІғмңјлЎң нҷ•мқёлҗҳм—ҲлӢӨ[11]. мқҙ кІ°кіјм—җм„ң histone deacetylase inhibitor м№ҳлЈҢк°Җ мғҲлЎңмҡҙ м№ҳлЈҢ л°©лІ•мңјлЎң кё°лҢҖлҗҳкі мһҲм§Җл§Ң м•„м§Ғ м№ҳлЈҢ нҡЁкіјлҠ” мһ…мҰқн•ҳм§Җ лӘ»н–ҲлӢӨ[12,13].
ліё мҰқлЎҖл“ӨмқҖ м •ліҙмқҳ м ңн•ңм җмқҙ мһҲм—ҲлӢӨ. мІ« лІҲм§ёлЎң м•„м§Ғ м№ҳлЈҢ мӨ‘ лҳҗлҠ” м№ҳлЈҢ мў…кІ° нӣ„ кІҪкіј кҙҖм°° мӨ‘мңјлЎң мғқмЎҙ кё°к°„, м№ҳлЈҢмқҳ нҡЁкіј л°Ҹ мҷ„м№ҳ м—¬л¶ҖлҘј нҸүк°Җн• мҲҳ м—Ҷм—ҲлӢӨ. 1лІҲ мҰқлЎҖмқҳ кІҪмҡ° 진лӢЁ нӣ„ 9к°ңмӣ”, 2лІҲ мҰқлЎҖмқҳ кІҪмҡ° 진лӢЁ нӣ„ 5к°ңмӣ”м§ё кІҪкіј кҙҖм°° мӨ‘мқҙлӢӨ. лҢҖл¶Җ분мқҳ нҷҳмһҗлҠ” мҰқмғҒ л°ңмғқ мқҙнӣ„ 1л…„ мқҙлӮҙлЎң мӮ¬л§қн•ҳмҳҖкі , нҸүк· мғқмЎҙ кё°к°„мқҖ 9.5к°ңмӣ”мқҙм—ҲлӢӨ[10]. к·ёмӨ‘ 비л¶Җ비лҸҷ мҳҒм—ӯмқҳ NMCм—җм„ңлҠ” нҸүк· мғқмЎҙ кё°к°„мқҙ 12к°ңмӣ”мқҙм—ҲлӢӨ. Bishopкіј Westra[4]мқҳ л…јл¬ём—җм„ңлҠ” 3лӘ…мқҳ нҷҳмһҗ лӘЁл‘җ мІҳмқҢ 진лӢЁ лӢ№мӢңм—җ мӣҗкІ© м „мқҙк°Җ м—Ҷм—ҲмңјлӮҳ мӮ¬л§қ лӢ№мӢңм—җлҠ” 3лӘ… лӘЁл‘җ мӣҗкІ© м „мқҙк°Җ нҷ•мқёлҗҳм—ҲлӢӨ. м№ҳлЈҢ мў…кІ° нӣ„м—җлҸ„ кІҪкіј кҙҖм°°мқ„ н•ҳл©ҙм„ң мһ¬л°ң л°Ҹ мӣҗкІ© м „мқҙм—җ лҢҖн•ң кҫёмӨҖн•ң нҸүк°Җк°Җ н•„мҡ”н•ҳкІ лӢӨ. л‘җ лІҲм§ёлЎң м„ёнҸ¬мң м „н•ҷм Ғ кІҖмӮ¬лҘј мӢңн–үн•ҳм§Җ м•Ҡм•ҳлӢӨ. NUT мң м „мһҗмҷҖ мһ¬л°°м—ҙмқ„ н•ң мң м „мһҗк°Җ м–ҙл–Ө кІғмқём§Җ нҷ•мқён• мҲҳ м—Ҷм—ҲлӢӨ. м•һм„ң м–ёкёүн•ң лҢҖлЎң BRD4-NUT NMCк°Җ 2/3 м •лҸ„лҘј м°Ём§Җн•ҳкі , BRD4 мҷёмқҳ лӢӨлҘё мң м „мһҗмҷҖ мһ¬л°°м—ҙмқ„ н•ң NUT variant NMCк°Җ 1/3 м •лҸ„лҘј м°Ём§Җн•ңлӢӨ[2]. French л“ұ[14]мқҖ мҙҲкё°м—җлҠ” NUT-variant NMCк°Җ BRD4-NUT NMCліҙлӢӨ лҚ” мўӢмқҖ мҳҲнӣ„лҘј ліҙмқёлӢӨкі ліҙкі н•ҳмҳҖмңјлӮҳ, мөңк·ј м—°кө¬ кІ°кіјм—җм„ңлҠ” м°Ёмқҙк°Җ м—ҶлӢӨкі ліҙкі н•ҳмҳҖлӢӨ[15]. н–Ҙнӣ„ м„ёнҸ¬мң м „н•ҷм Ғ кІҖмӮ¬лҘј мӢңн–үн•ҳм—¬ мң м „мһҗ м°Ёмқҙм—җ л”°лҘё NMCмқҳ 진н–ү м–‘мғҒмқҳ м°ЁмқҙлҘј 분м„қн• н•„мҡ”к°Җ мһҲкІ лӢӨ.
ліё мҰқлЎҖл“ӨмқҖ 비л¶Җ비лҸҷ мҳҒм—ӯм—җм„ң NMCмқҳ 진лӢЁкіј м№ҳлЈҢ кіјм •мқ„ мһҳ ліҙм—¬мЈјлҠ” мўӢмқҖ мҳҲл“ӨмқҙлӢӨ. 추нӣ„ мһҘкё°м Ғмқё 추м Ғ кҙҖм°°мқ„ нҶөн•ҙ м№ҳлЈҢ кІ°кіјлҘј 분м„қн• н•„мҡ”к°Җ мһҲкІ лӢӨ. NMCлҠ” л“ңл¬јкі лҶ’мқҖ мӮ¬л§қлҘ мқ„ ліҙмқҙм§Җл§Ң лі‘лҰ¬мЎ°м§Ғн•ҷм Ғ кІҖмӮ¬л§ҢмңјлЎңлҠ” 진лӢЁмқҙ м–ҙл Өмҡҙ м§ҲнҷҳмқҙлӢӨ. мқҙм—җ ліё м Җмһҗл“ӨмқҖ 비л¶Җ비лҸҷ мҳҒм—ӯм—җм„ң л°ңмғқн•ң м Җ분нҷ” лҳҗлҠ” лҜёл¶„нҷ”м•”мў…м—җ лҢҖн•ҙ NUT л©ҙм—ӯмЎ°м§Ғнҷ”н•ҷкІҖмӮ¬лҘј мӢңн–үн•ҳм—¬ л№ лҘё 진лӢЁкіј м№ҳлЈҢк°Җ мӢңн–үлҗҳм–ҙм•ј н•Ёмқ„ к°•мЎ°н•ңлӢӨ.