ņä£ ļĪĀ
ļ¦īņä▒ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņØĆ ņĀÉļ¦ēņ£╝ļĪ£ ĻĄ¼ņä▒ļÉ£ ņżæņØ┤Ļ░Ģ ļé┤ļĪ£ Ļ░üĒÖöĒĢ£ ĒÄĖĒÅēņāüĒö╝Ļ░Ć ņ╣©ņ×ģĒĢśņŚ¼ Ļ░üņ¦ł(keratin)ņØä ņČĢņĀüĒĢśļ®┤ņä£ ņŻ╝ņ£äņØś Ļ│©ņĪ░ņ¦üņØä ĒīīĻ┤┤ĒĢśļŖö ņ¦łĒÖśņØ┤ļŗż. ņ¦äņŻ╝ņóģņØś ņ¦äļŗ©ņØĆ ļīĆļČĆļČäņØś Ļ▓ĮņÜ░ ņØ┤Ļ▓Į, Ēśäļ»ĖĻ▓Į ļśÉļŖö ņØ┤ļé┤ņŗ£Ļ▓ĮņØä ĒåĄĒĢ┤ ņżæņØ┤ņŚÉ ņ׳ļŖö ļ░▒ņāēņØś ņóģļ¼╝ņØä ĒÖĢņØĖĒĢ©ņ£╝ļĪ£ņŹ© ņØ┤ļŻ©ņ¢┤ņ¦Ćļ®░, ļ░®ņé¼ņäĀĒĢÖņĀü Ļ▓Ćņé¼ļĪ£ļŖö ņĖĪļæÉĻ│© ņĀäņé░ĒÖöļŗ©ņĖĄņ┤¼ņśü(temporal bone CT, TBCT)ņØä ņŗ£Ē¢ēĒĢśņŚ¼ ņŚ╝ņ”ØņØ┤ļéś ņ¦äņŻ╝ņóģņØś ļ▓öņ£ä, ņØ┤ņåīĻ│© ļ░Å ņŻ╝ļ│Ć Ļ│©ņĪ░ņ¦üņØĖ Ļ│ĀņŗżĻ░£(scutum), ņĢłļ®┤ņŗĀĻ▓ĮĻ┤Ć, Ļ│©ļ»ĖļĪ£, ņ£ĀļÅīĻ│ĀņŗżĻ░£(tegmen) ļō▒ņØś ĒīīĻ┤┤, ĻĘĖļ”¼Ļ│Ā ņ£Āņ¢æļÅÖĻ│╝ Sņāü ņĀĢļ¦źļÅÖņØś Ēü¼ĻĖ░ņÖĆ ņ£äņ╣ś ļō▒ņŚÉ ļīĆĒĢ£ ņĀĢļ│┤ļź╝ ņ¢╗Ļ▓ī ļÉ£ļŗż. ĻĘĖļ¤¼ļéś, ņØ┤Ļ▓ĮņŚÉņä£ ĒŖ╣ņ¦ĢņĀüņØĖ ņåīĻ▓¼ņØä ļ│┤ņØ┤ņ¦Ć ņĢŖĻ▒░ļéś, TBCTņāüņŚÉņä£ Ļ│©ĒīīĻ┤┤ļź╝ ļ¬ģĒÖĢĒĢśĻ▓ī Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåļŖö ņ┤łĻĖ░ņØś ļ│æļ│Ć, Ēś╣ņØĆ ņČöņ▓┤ ņ▓©ļČĆņŚÉ ļ░£ņāØĒĢ£ ņ¦äņŻ╝ņóģņØś Ļ▓ĮņÜ░ ņ¦äļŗ©ņØ┤ ņ¢┤ļĀżņÜĖ ņłś ņ׳ņ£╝ļ®░, ņłśņłĀ Ēøä ņ×¼ļ░£ĒĢ£ Ļ▓ĮņÜ░ņŚÉļÅä ņłĀĒøä Ļ│Āļ¦ēņØś ļ╣äĒøäļĪ£ ņØĖĒĢśņŚ¼ ĻĘĖ ņ¦äļŗ©ņØ┤ ņ¢┤ļĀżņøī ĒĢäņÜöņŗ£ ņŗ£ĒŚśņĀü Ļ│Āņŗż Ļ░£ļ░®ņłĀņØä ņŗ£Ē¢ēĒĢśĻĖ░ļÅä ĒĢ£ļŗż[1,2].
ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü(magnetic resonance imaging, MRI)ņØś Ļ▓ĮņÜ░ ņ¦äņŻ╝ņóģņØĆ ļŗżņ¢æĒĢ£ ņŗĀĒśĖĻ░ĢļÅäļź╝ ļ│┤ņØ╝ ņłś ņ׳ņ£╝ļéś, ņØ╝ļ░śņĀüņ£╝ļĪ£ T1 Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ļćīņŗżņ¦łĻ│╝ ļ╣äņŖĘĒĢśĻ▒░ļéś ņĢĮĻ░ä ļé«ņØĆ ņŗĀĒśĖĻ░ĢļÅäļź╝ ļ│┤ņØ┤Ļ│Ā T2 Ļ░ĢņĪ░ņśüņāüņŚÉņä£ļŖö ļŗżņ¢æĒĢ£ ņŗĀĒśĖĻ░ĢļÅäļź╝ ļ│┤ņØ┤ļ®░ ņĪ░ņśüņĀ£ ņŻ╝ņ×ģ Ēøä ļé┤ļČĆļŖö ņĪ░ņśü ņ”ØĻ░ĢņØä ļ│┤ņØ┤ņ¦Ć ņĢŖļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż.
ņĄ£ĻĘ╝ņŚÉ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņØś ņ¦äļŗ©ņŚÉ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāü(diffusion-weighted image)ņØä ņØ┤ņÜ®ĒĢ£ ņŚ░ĻĄ¼Ļ░Ć ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[3]. ņØ┤ ņżæ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāü(PROPELLER diffusion-weighted image)ņØ┤ļ×Ć multishot fast spin-echo ĻĖ░ļ░śņŚÉ ļÅģĒŖ╣ĒĢ£ K-space sampling(Periodically Rotated Overlapping ParallEL Lines with Enhanced Reconstruction; General Electric) ļ░®ļ▓Ģņ£╝ļĪ£ ņĄ£ĻĘ╝ ņ×äņāüņŚÉ ņåīĻ░£ļÉśņ¢┤ ĻĘĖ ņ£ĀņÜ®ņä▒ņŚÉ Ļ┤ĆĒĢ£ ĒÜ©Ļ│╝ ļ░Å ņØæņÜ®ņŚÉ ļīĆĒĢśņŚ¼ ļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ░Ć ņØ┤ļŻ©ņ¢┤ņĀĖ ņÖöļŗż[4,5]. ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØĆ Ļ│ĀņåŹ ņŖżĒĢĆ ņŚÉņĮö(fast spin echo)ņŚÉ ĻĖ░ļ░śņØä ļæÉĻ│Ā ņ׳ņ£╝ļ»ĆļĪ£ ĻĖ░ņĪ┤ņØś ņŚÉņĮöĒÅēļ®┤(echo-planar) ņśüņāüņŚÉ ĻĖ░ļ░śņØä ļæö ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉ ļ╣äĒĢ┤ ļīĆņāüņØś ņØ┤ņ¦łņä▒(inhomogenity)ņ£╝ļĪ£ ņØĖĒĢ£ susceptibility artifactņØś ņśüĒ¢źņØä ļŹ£ ļ░øĻĖ░ ļĢīļ¼ĖņŚÉ ņ×äņāüņĀüņ£╝ļĪ£ ļŹö ņ£ĀņÜ®ĒĢśĻ▓ī ņé¼ņÜ®ĒĢĀ ņłś ņ׳ņ£╝ļ®░, multishot ĻĖ░ļ▓ĢņØä ņé¼ņÜ®ĒĢśļ»ĆļĪ£ ņĀĢņāü ņŗĀĒśĖļīĆņ×ĪņØīļ╣ä(signal-to-noise ratio)ņŚÉņä£ Ļ│ĀĒĢ┤ņāüļÅäņØś ņśüĒ¢źņØä ļŗżļŻ©ĻĖ░ ņē¼ņÜ┤ ņןņĀÉņØ┤ ņ׳ļŗż[6].
Koot ļō▒[7]ņØĆ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ĻĖ░ņĪ┤ņØś ņ┤¼ņśü ĻĖ░ļ▓Ģņ£╝ļĪ£ļŖö ņ¦äļŗ©ņØ┤ ņ¢┤ļĀżņÜ┤ ļćīņØś ņĖĪļćīņŗżņŚÉ ļ░£ņāØĒĢ£ ņ£ĀĒæ£Ēö╝ņóģņØä ņ¦äļŗ©ĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢ£ ļ░öĻ░Ć ņ׳ļŗż. ņ£ĀĒæ£Ēö╝ņóģņØĆ ņ¦äņŻ╝ņóģĻ│╝ ļÅÖņØ╝ĒĢ£ ņ╝ĆļØ╝Ēŗ┤ ņä▒ļČäņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░ ņżæņØ┤ņŚÉ ļ░£ņāØĒĢśņśĆņØä Ļ▓ĮņÜ░ ņ¦äņŻ╝ņóģņ£╝ļĪ£ ļČłļ”¼ĻĖ░ļÅä ĒĢ£ļŗż.
ņØ┤ņŚÉ ņĀĆņ×ÉļōżņØĆ ņĄ£ĻĘ╝ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņŚÉ ņ׳ņ¢┤ ĻĘĖ ņ¦äļŗ©ņĀü Ļ░Ćņ╣śļź╝ ņĢīņĢäļ│┤Ļ│Ā, ņśüņāüĻ│╝ ļ│æļ”¼ņĪ░ņ¦üĒĢÖņĀü ņåīĻ▓¼Ļ│╝ņØś Ļ┤ĆļĀ©ņä▒ņØä ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢśņśĆļŗż.
ļīĆņāü ļ░Å ļ░®ļ▓Ģ
2005ļģä 1ņøöļČĆĒä░ 2015ļģä 9ņøöĻ╣īņ¦Ć Ļ│äļ¬ģļīĆĒĢÖĻĄÉ ļÅÖņé░ņØśļŻīņøÉ ņØ┤ļ╣äņØĖĒøäĻ│╝ĒĢÖ ĻĄÉņŗżņŚÉņä£ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņØ┤ ņØśņŗ¼ļÉśņ¢┤ ņłĀņĀä MRIļź╝ ņ┤¼ņśüĒĢ£ 67ļ¬ģņØś ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ ĒøäĒ¢źņĀüņ£╝ļĪ£ ņŚ░ĻĄ¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. 67ļ¬ģņØś ĒÖśņ×É ņżæ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ ĒÖśņ×ÉļŖö 51ļ¬ģņØ┤ņŚłĻ│Ā, ļ╣äņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ ĒÖśņ×ÉļŖö 16ļ¬ģņØ┤ņŚłļŗż. 51ļ¬ģņØś ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ ĒÖśņ×ÉņŚÉļŖö ņäĀņ▓£ņä▒ ņ¦äņŻ╝ņóģņØ┤ 4ņśł, Ēøäņ▓£ņä▒ ņ¦äņŻ╝ņóģņØ┤ 47ņśłņśĆņ£╝ļ®░, 16ļ¬ģņØś ļ╣äņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņŚÉļŖö ņĮ£ļĀłņŖżĒģīļĪż ņ£ĪņĢäņóģņØ┤ 3ņśł, ļ¦īņä▒ ņ£ĪņĢäņóģņä▒ ņżæņØ┤ņŚ╝ņØ┤ 13ņśł Ļ┤Ćņ░░ļÉśņŚłļŗż. ņ¢æ ĻĄ░ņŚÉņä£ņØś ņä▒ļ│ä, ņŚ░ļĀ╣, ļ░®Ē¢ź, ļ│æļ│ĆņØś Ēü¼ĻĖ░ļŖö ĒåĄĻ│äĒĢÖņĀüņ£╝ļĪ£ ņ£ĀņØśĒĢ£ ņ░©ņØ┤ļź╝ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż(Table 1).
ĒÖśņ×ÉļōżņØĆ ļ¬©ļæÉ ņłĀņĀäņŚÉ TBCT, 3T MRI(Sigma Excite, General Electric, Milwaukee, WI, USA) ĻĖ░ĻĖ░ņŚÉņä£ T1 Ļ░ĢņĪ░ņśüņāü, T2 Ļ░ĢņĪ░ņśüņāüĻ│╝ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. TBCTļŖö 0.8 mmņØś Ļ░äĻ▓®ņ£╝ļĪ£ ņ┤¼ņśüļÉśņŚłņ£╝ļ®░ T1, T2 Ļ░ĢņĪ░ņśüņāüņØĆ 1 mm Ļ░äĻ▓®ņ£╝ļĪ£, ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØĆ 3 mm Ļ░äĻ▓®ņ£╝ļĪ£ ņ┤¼ņśüļÉśņŚłĻ│Ā, ļ¬©ļōĀ ņśüņāüņØĆ ņČĢļ®┤(axial plane)ņŚÉņä£ Ļ┤Ćņ░░ĒĢśņśĆļŗż.
ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ņżæņØ┤Ļ░ĢņŚÉ ļćīņØś ņŗżņ¦łĻ│╝ ĒÖĢņŚ░Ē׳ ĻĄ¼ļ│äļÉśļŖö Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉ£ Ļ▓ĮņÜ░ MRIņāüņØś ņ¢æņä▒ ņåīĻ▓¼ņ£╝ļĪ£ ĒīÉļŗ©ĒĢśņśĆĻ│Ā, ņśüņāüņØĆ ĒĢ£ ļ¬ģņØś ņśüņāüņØśĒĢÖĻ│╝ ņĀäļ¼ĖņØśņØś ĒīÉļÅģņØä ļ░øņĢä ņłĀņĀä ņśüņāü ņåīĻ▓¼ļ¦īņ£╝ļĪ£ ņ¦äņŻ╝ņóģņØś ņ£Āļ¼┤ļź╝ ņśłņĖĪĒĢśņśĆļŗż. ļśÉĒĢ£ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśļŖö ļ¬©ņ¢æņŚÉ ļö░ļØ╝ 2Ļ░£ņØś ĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż. MRIņāü Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖĻ░Ć TBCTņāüņØś ņŚ░ļČĆ ņĪ░ņ¦ü ņØīņśüņØä ĻĘĖļīĆļĪ£ ļ░śņśüĒĢśņŚ¼ ņĀäņ▓┤ņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ļź╝ IĻĄ░ņ£╝ļĪ£, TBCTņŚÉņä£ Ļ┤Ćņ░░ļÉśļŖö ņŚ░ļČĆ ņĪ░ņ¦ü ņØīņśüņØ┤ Ļ░Ćņןņ×Éļ”¼(rim)ņØś Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖļ¦ī ļ│┤ņØ┤Ļ│Ā, ļé┤ļČĆņŚÉļŖö ņĀĆņØīņśüņØś ņŗĀĒśĖļź╝ ļ│┤ņØ╝ Ļ▓ĮņÜ░ IIĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż.
ņłśņłĀņØĆ ĒĢ£ ļ¬ģņØś ņØ┤ļ╣äņØĖĒøäĻ│╝ ņĀäļ¼ĖņØśņŚÉ ņØśĒĢ┤ ņŗ£Ē¢ēļÉśņŚłņ£╝ļ®░, ļ¬©ļōĀ ĒÖśņ×ÉļŖö ņĀäņŗĀļ¦łņĘ©ĒĢśņŚÉ Ļ│Āņŗż ņä▒ĒśĢņłĀ ļ░Å ņ£Āņ¢æļÅīĻĖ░ ņéŁĻ░£ņłĀņØä ņŗ£Ē¢ēĒĢśņśĆļŗż. ņłĀ ņżæņŚÉ ņśüņāü ņåīĻ▓¼Ļ│╝ ņØ╝ņ╣śĒĢśļŖö ļČĆņ£äņŚÉņä£ ņ¦äņŻ╝ņóģņ£╝ļĪ£ ņāØĻ░üļÉśļŖö ļ░▒ņāē ņóģļ¼╝ņØś ņĪ┤ņ×¼ ņŚ¼ļČĆļź╝ ņ£ĪņĢłņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņśĆĻ│Ā ĻĘĖ ļČĆņ£äņŚÉņä£ ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ļ│æļ”¼ ņĪ░ņ¦ü Ļ▓Ćņé¼ņāü Ļ░üņ¦ł(keratin)ņØ┤ Ļ┤Ćņ░░ļÉĀ Ļ▓ĮņÜ░ ņ¦äņŻ╝ņóģņ£╝ļĪ£ ĒÖĢņ¦äĒĢśņśĆļŗż.
ņśüņāü ĒīÉļÅģ ņåīĻ▓¼Ļ│╝ ņłśņłĀ ņåīĻ▓¼, ĻĘĖļ”¼Ļ│Ā ņĄ£ņóģ ļ│æļ”¼ ņĪ░ņ¦üĒĢÖņĀü Ļ▓Ćņé¼ Ļ▓░Ļ│╝ļź╝ ĒÖĢņØĖĒĢśņŚ¼, ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ĒåĄĒĢ£ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ņä£ņØś ļ»╝Ļ░ÉļÅä(sensitivity)ņÖĆ ĒŖ╣ņØ┤ļÅä(specifivity), ņ¢æņä▒ ņśłņĖĪļźĀ(positive predictable value, PPV)Ļ│╝ ņØīņä▒ ņśłņĖĪļźĀ(negative predictable value, NPV)ņØä ņĪ░ņé¼ĒĢśņśĆļŗż.
Ļ▓░ Ļ│╝
ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØś ņ¦äļŗ©ņĀü Ļ░Ćņ╣ś
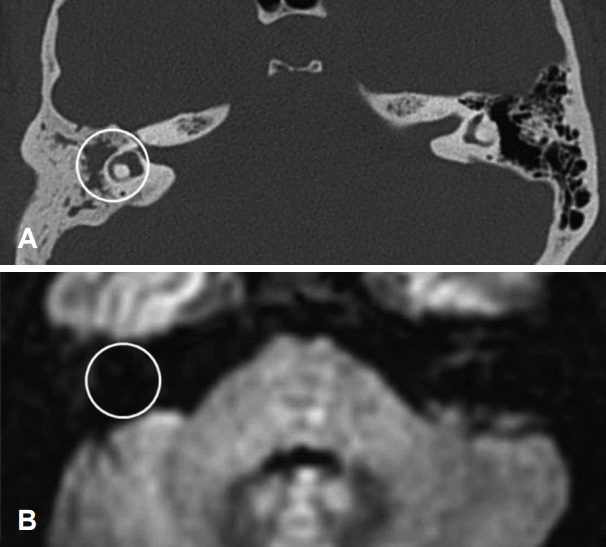
ņ¦äņŻ╝ņóģņØś Ļ▓ĮņÜ░ ņłĀņĀä ņŗ£Ē¢ēĒĢ£ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ņŻ╝ņ£ä ļćī ņŗżņ¦łĻ│╝ ĒÖĢņŚ░Ē׳ ĻĄ¼ļ│äļÉśļŖö ĒŖ╣ņ¦ĢņĀüņØĖ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłņ£╝ļéś ļ╣äņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņŚÉņä£ļŖö Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåņŚłļŗż(Fig. 1).
ņ┤Ø 67ļ¬ģņØś ĒÖśņ×É ņżæ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņØ┤ ņĄ£ņóģņĀüņ£╝ļĪ£ ņ¦äļŗ©ļÉ£ 51ļ¬ģņØś ĒÖśņ×É 48ļ¬ģņŚÉņä£ ņŻ╝ņ£ä ļćī ņŗżņ¦łĻ│╝ ĻĄ¼ļ│äļÉśļŖö Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłĻ│Ā, ņ¦äņŻ╝ņóģņØ┤ ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖņĢśļŹś 16ļ¬ģņØś ĒÖśņ×ÉņŚÉņä£ļŖö ļ¬©ļæÉ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖĻ░Ć ļéśĒāĆļéśņ¦Ć ņĢŖņĢśļŗż(Table 2). ļö░ļØ╝ņä£ ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņĪ░ņé¼ļÉ£ ļ»╝Ļ░ÉļÅä(sensitivity)ļŖö 94.1%ņśĆĻ│Ā, ĒŖ╣ņØ┤ļÅä(specificity)ļŖö 100%ņśĆņ£╝ļ®░, ņ¢æņä▒ ņśłņĖĪļźĀ(PPV)Ļ│╝ ņØīņä▒ ņśłņĖĪļźĀ(NPV)ļÅä Ļ░üĻ░ü 100%, 84.2%ļĪ£ ļéśĒāĆļé¼ļŗż.
MRI ņśüņāüņØś ĒśĢĒā£ņŚÉ ļö░ļźĖ ļČäļźśņÖĆ ļ│æļ”¼ņĪ░ņ¦üĒĢÖņĀü ņåīĻ▓¼
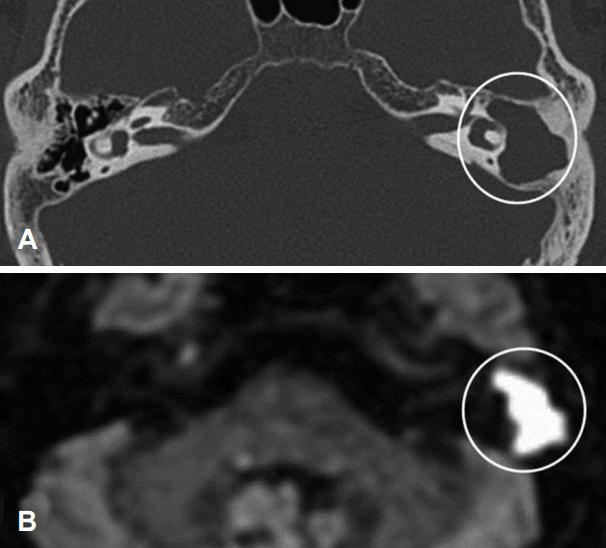
MRIļź╝ ļČäņäØĒĢśņŚ¼ ļ│┤ņĢśņØä ļĢī Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖņØś ĒśĢĒā£ņŚÉ ļö░ļØ╝ ļæÉ Ļ░Ćņ¦Ć ĻĄ░ņ£╝ļĪ£ ļČäļźśļź╝ ņŗ£Ē¢ēĒĢśņśĆļŗż. TBCTņāüņØś ņŚ░ļČĆņĪ░ņ¦ü ņØīņśüņØ┤ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ĻĘĖļīĆļĪ£ Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖļĪ£ ļ░śņśüļÉśņ¢┤ ņĀäņ▓┤ņĀüņ£╝ļĪ£ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ ļ│┤ņØĖ Ļ▓ĮņÜ░Ļ░Ć 43ņśłņŚÉņä£ Ļ┤Ćņ░░ļÉśņŚłņ£╝ļ®░ ņØ┤ļź╝ IĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż(Fig. 2). ĻĘĖļ”¼Ļ│Ā TBCTņŚÉņä£ Ļ┤Ćņ░░ļÉśļŖö ņŚ░ļČĆ ņĪ░ņ¦ü ņØīņśüņØ┤ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ Ļ░Ćņןņ×Éļ”¼ļ¦ī Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśĻ│Ā ļé┤ļČĆņØś ņĀĆņØīņśüņØä ļ│┤ņØĖ Ļ▓ĮņÜ░Ļ░Ć 6ņśłņŚÉņä£ ņ׳ņŚłņ£╝ļ®░ ņØ┤ļź╝ IIĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņśĆļŗż(Fig. 3).
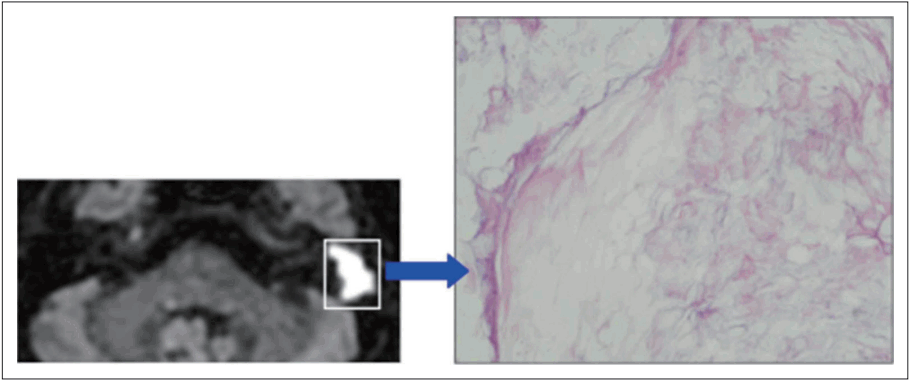
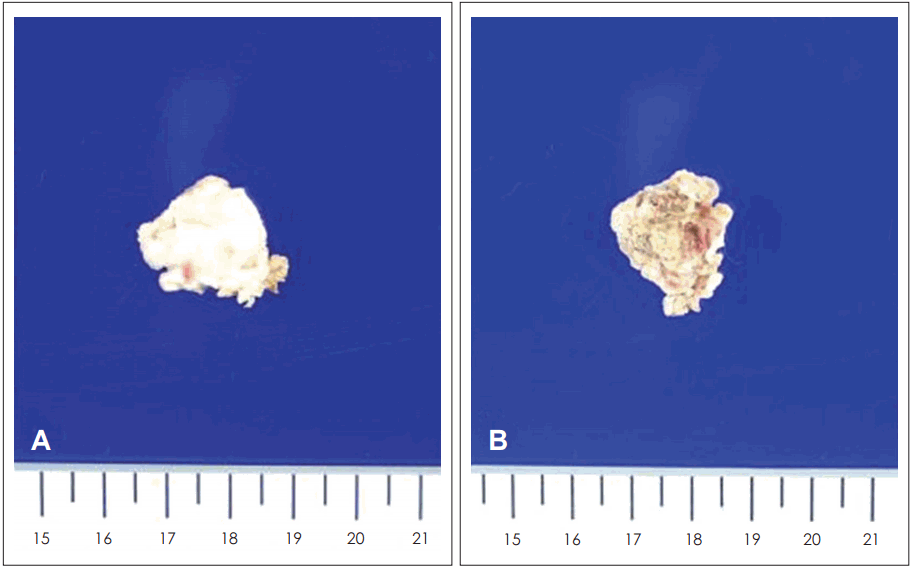
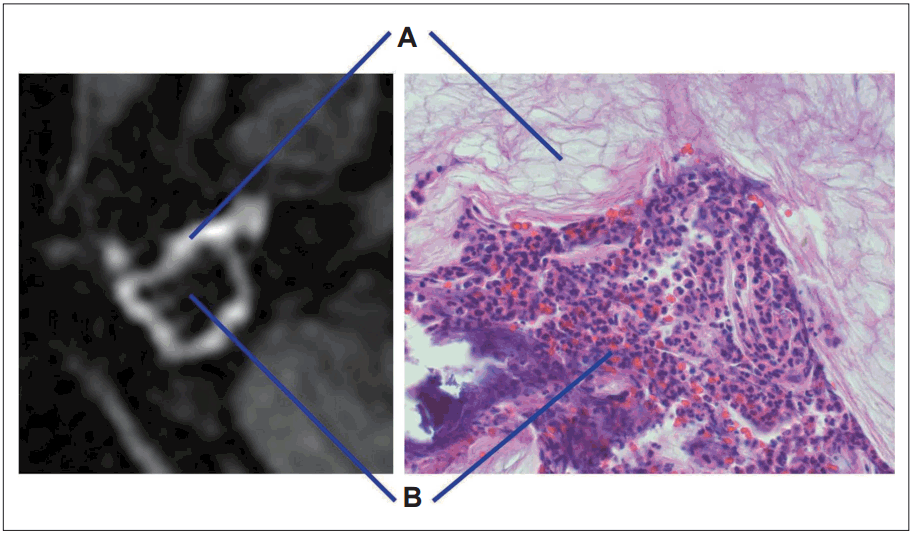
ļśÉĒĢ£ ļæÉ ĻĄ░ņØś ņĪ░ņ¦üĒĢÖņĀü ņ░©ņØ┤ļź╝ ņĢīņĢäļ│┤ĻĖ░ ņ£äĒĢ┤ ļæÉ ĻĄ░ņØś ļ│æļ”¼ĒĢÖņĀü ņåīĻ▓¼ņØä Ļ┤Ćņ░░ĒĢ┤ ļ│┤ņĢśļŗż. IĻĄ░ņØś Ļ▓ĮņÜ░ ņŚ░ļČĆņĪ░ņ¦ü ņØīņśüņØ┤ ļ¬©ļæÉ ņ¦äņŻ╝ņóģņØś ĻĖ░ņ¦łņØĖ Ļ░üņ¦ł(keratin)ļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ņØīņØä ņĢī ņłśĻ░Ć ņ׳ņŚłĻ│Ā(Fig. 4), 2ĻĄ░ņØś Ļ▓ĮņÜ░ ņ£ĪņĢłņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśņŚ¼ ļ│┤ņĢśņØä ļĢī Ēæ£ļ®┤ņØĆ ĒÜīļ░▒ņāēņØś ņ¦äņŻ╝ņóģ ĻĖ░ņ¦łņØ┤ ļæśļ¤¼ņŗĖĻ│Ā ņ׳ļŖö ņ¢æņāüņØ┤ņŚłņ£╝ļ®░, ļé┤ļČĆņØś ņĀłļŗ©ļ®┤ņØĆ ĒÖöļåŹņä▒(suppurative)ņØś ļ│æļ│ĆņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 5). Ēśäļ»ĖĻ▓ĮņĀü ņåīĻ▓¼ņŚÉņä£ļÅä Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖļź╝ ļ│┤ņØĖ ņŻ╝ļ│Ć ļČĆņ£äĻ░Ć ņ¦äņŻ╝ņóģņØś ņŗżņ¦łņØ┤ņŚłĻ│Ā, ļé┤ļČĆņŚÉ ĒśĖņżæĻĄ¼(neutrophil)Ļ░Ć ņÜ┤ņ¦æĒĢ£ ĒÖöļåŹņä▒ņØś ļ│ĆĒÖöĻ░Ć ņ׳ņØīņØä ņĢī ņłś ņ׳ņŚłļŗż(Fig. 6).
Ļ│Ā ņ░░
ņ¦äņŻ╝ņóģņØĆ ņ×äņāüņĀüņ£╝ļĪ£ ņØ┤Ļ▓Į ņåīĻ▓¼ņØä ĒåĄĒĢ┤ ņØśņŗ¼ĒĢśĻ▓ī ļÉśĻ│Ā, TBCTļéś MRIļŖö ļ│æļ│ĆņØś ļ▓öņ£ä Ēś╣ņØĆ ņØ┤ņåīĻ│©ņØ┤ļéś ņŻ╝ņ£ä Ļ│©ņĪ░ņ¦üņØś ļ»Ėļ×Ć ĒīīĻ┤┤ ļō▒ņØś ņČöĻ░ĆņĀüņØĖ ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢśļŖö ļ│┤ņĪ░ņĀüņØĖ ņŚŁĒĢĀņØä ĒĢśĻ▓ī ļÉśļ®░, TBCTļéś MRIļ¦īņ£╝ļĪ£ ņ¦äņŻ╝ņóģņØä ņ¦äļŗ©ĒĢśļŖö ļŹ░ļŖö ļģ╝ļ×ĆņØś ņŚ¼ņ¦ĆĻ░Ć ņ׳ņ¢┤ ņÖöļŗż. ĒŖ╣Ē׳ ņ¦äņŻ╝ņóģņØś ņłśņłĀ ņŗ£ ņÖĖņØ┤ļÅä Ēøäļ▓ĮņØä ļ│┤ņĪ┤ĒĢ£ Ļ▓ĮņÜ░ņŚÉļŖö ņ×öļźśņä▒ ņ¦äņŻ╝ņóģņØ┤ 35%[8], ņ×¼ļ░£ņä▒ ņ¦äņŻ╝ņóģņØ┤ 18%[9]ņŚÉņä£ Ļ┤Ćņ░░ļÉ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśņ¢┤ņ¦äļŗż. Ļ▓īļŗżĻ░Ć ņłĀĒøäņŚÉ ļ░£ņāØĒĢ£ Ļ▓ĮņÜ░ņŚÉļŖö Ļ│Āļ¦ēņØś ņāüņ▓śļéś ļ╣äĒøäļĪ£ ņØĖĒĢśņŚ¼ ņØ┤ĒĢÖņĀü Ļ▓Ćņé¼ļ¦īņ£╝ļĪ£ ņ×¼ļ░£ņØä ļ╣©ļ”¼ ņĢīņĢäļé┤ĻĖ░ļŖö ļ¦żņÜ░ ĒלļōĀ Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[10].
ņłśņłĀĒøä ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö ņ×¼ļ░£ņä▒ Ēś╣ņØĆ ņ×öļźśņä▒ ņ¦äņŻ╝ņóģņŚÉ ļīĆĒĢ£ ņØśņŗ¼ņØĆ ļĢīļĢīļĪ£ ņØ┤ļŻ©(otorrhea)ļź╝ ĒåĄĒĢśņŚ¼ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż. ļ¦īņĢĮ ņĀüņĀłĒĢ£ ņĢĮļ¼╝ ņ╣śļŻīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņØ┤ļŻ©Ļ░Ć ņ¦ĆņåŹļÉĀ Ļ▓ĮņÜ░ņŚÉļŖö ņ¦äņŻ╝ņóģņØ┤ ļ░£ņāØĒĢśņśĆņØä Ļ░ĆļŖźņä▒ņØä ņśłņĖĪĒĢĀ ņłś ņ׳ņ£╝ļ®░, ļ░śļīĆļĪ£ ņØ┤ļŻ©Ļ░Ć ņĢĮļ¼╝ ņ╣śļŻī ņØ┤Ēøä ņĪ░ņĀłļÉśņŚłņØä Ļ▓ĮņÜ░ņŚÉļŖö ļ¦īņä▒ ĒÖöļåŹņä▒ ņżæņØ┤ņŚ╝ņØ╝ Ļ░ĆļŖźņä▒ņØ┤ ļåÆņØä Ļ▓āņØ┤ļØ╝Ļ│Ā ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ¤¼ļéś ņØ┤ Ļ▓ĮņÜ░ņŚÉļÅä ņŚŁņŗ£ ņ¦äņŻ╝ņóģņØä ņÖäņĀäĒ׳ ļ░░ņĀ£ĒĢĀ ņłś ņŚåņ£╝ļ»ĆļĪ£ ņŗ£ĒŚśņĀüņØĖ Ļ│Āņŗż Ļ░£ļ░®ņłĀņØä ņŗ£Ē¢ēĒĢśĻ▒░ļéś ņČöĻ░ĆņĀüņØĖ ļ░®ņé¼ņäĀĒĢÖņĀü Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż[9]. ļö░ļØ╝ņä£ ņØ┤ļ¤¼ĒĢ£ Ļ▓ĮņÜ░ ņ¦äņŻ╝ņóģņØä Ļ░Éļ│äĒĢśĻĖ░ ņ£äĒĢ┤ ņŚ¼ļ¤¼ Ļ░Ćņ¦Ć ļ░®ņé¼ņäĀĒĢÖņĀü Ļ▓Ćņé¼ļōżņØ┤ ņŗ£Ē¢ēļÉśĻ│Ā ļ░£ņĀäļÉśņ¢┤ ņÖöļŗż.
ThomassinĻ│╝ Braccini [11]ļŖö ĻĘĖļōżņØś ņŚ░ĻĄ¼ņŚÉņä£ TBCTņāü ņŚ░ļČĆņĪ░ņ¦ü ņØīņśüņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ ļ¬©ļōĀ ĒÖśņ×ÉņŚÉņä£ ņ×¼ļ░£ņä▒ Ēś╣ņØĆ ņ×öļźśņä▒ ņ¦äņŻ╝ņóģņØä Ļ┤Ćņ░░ĒĢĀ ņłś ņŚåņ¢┤ 100%ņØś ņØīņä▒ ņśłņĖĪļźĀ(NPV)ņØä Ļ░Ćņ¦äļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż. ļö░ļØ╝ņä£ Williams ļō▒[12]ņØĆ TBCTņŚÉņä£ ņŚ░ļČĆņĪ░ņ¦ü ņØīņśüņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņØä Ļ▓ĮņÜ░ņŚÉļŖö ņČöĻ░ĆņĀüņØĖ Ļ▓Ćņé¼ļéś ņłśņłĀņØä ĒĢĀ ĒĢäņÜöĻ░Ć ņŚåņØä Ļ▓āņØ┤ļØ╝Ļ│Ā ņāØĻ░üĒĢśņśĆļŗż. ĻĘĖļ¤¼ļéś TBCTņŚÉņä£ ņŚ░ļČĆņĪ░ņ¦ü ņØīņśüņØ┤ Ļ┤Ćņ░░ļÉśņŚłņØä Ļ▓ĮņÜ░ TBCT ņåīĻ▓¼ļ¦īņ£╝ļĪ£ļŖö Ļ┤Ćņ░░ļÉ£ ļ│æļ│ĆņØ┤ ņ£ĪņĢäņóģņØ┤ļéś ņĮ£ļĀłņŖżĒģīļĪż ņ£ĪņĢäņóģ Ēś╣ņØĆ ļ╣äĒøäļÉ£ ņĀÉļ¦ēĻ│╝ Ļ░Éļ│äņØ┤ ņ¢┤ļĀżņÜ░ļ®░ ņ¦äņŻ╝ņóģņØ┤ ņ׳ņØīņØä ņśłņĖĪĒĢśļŖö ļŹ░ ļÅäņøĆņØä ņżä ņłś ņ׳ļŖö ņŻ╝ļ│Ć Ļ│©ņØś ļ»Ėļ×Ć ļō▒ņØś ņåīĻ▓¼ļÅä ņłĀĒøäņŚÉļŖö ĻĘĖ ņŗĀļó░ļÅäĻ░Ć ļ¢©ņ¢┤ņ¦Éņ£╝ļĪ£ ņØĖĒĢ┤ ļé«ņØĆ ņ¢æņä▒ ņśłņĖĪļźĀ(PPV)ņØä Ļ░Ćņ¦ĆĻ▓ī ļÉ£ļŗż[13]. ņØ┤ ņÖĖņŚÉļÅä ņłĀĒøäņŚÉ ļ░£ņāØĒĢ£ ņ¦äņŻ╝ņóģņŚÉ ņ׳ņ¢┤ TBCTņØś ņ¦äļŗ©ņĀü ņ£ĀņÜ®ņä▒ņŚÉ ļīĆĒĢ┤ ļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ░Ć ņ׳ņ¢┤ ņÖöņ£╝ļ®░ ļ»╝Ļ░ÉļÅäļź╝ 48~54%, ĒŖ╣ņØ┤ļÅäļź╝ 29~41%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż[11,14,15].
MRIņØś Ļ▓ĮņÜ░ņŚÉļŖö ņłśņłĀņØä ĒĢśņ¦Ć ņĢŖņØĆ Ļ▓ĮņÜ░ņŚÉ ņ¦äņŻ╝ņóģĻ│╝ ļŗżļźĖ ņŚ╝ņ”Øņä▒ ļ│ĆĒÖöļź╝ Ļ░Éļ│äĒĢĀ ņłś ņ׳ņ£╝ļéś, ņłĀĒøä ļ│Ćņä▒ņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ņŚÉļŖö ņŚŁņŗ£ļéś ĻĘĖ ņĀĢĒÖĢļÅäĻ░Ć ļ¢©ņ¢┤ņ¦ĆļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ®░ ĻĖ░ņĪ┤ņŚÉ ņŗ£Ē¢ēļÉśņ¢┤ ņś© ņØ╝ļ░śņĀüņØĖ pulse sequenceņØś T1, T2 Ļ░ĢņĪ░ņśüņāüņØĆ ņ¦äņŻ╝ņóģĻ│╝ ļŗżļźĖ ņŚ░ņĪ░ņ¦ü Ēś╣ņØĆ ņĀÉņĢĪņä▒ ļČäļ╣äļ¼╝ņØä Ļ░Éļ│äĒĢśņ¦Ć ļ¬╗ĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[16].
ļö░ļØ╝ņä£ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ņé¼ņÜ®ĒĢśņ¦Ć ņĢŖļŖö ĻĖ░ņĪ┤ņØś MRIļź╝ ņé¼ņÜ®ĒĢ£ Ļ▓ĮņÜ░ ņłśņłĀĒøäņŚÉ ļ░£ņāØĒĢ£ ņ¦äņŻ╝ņóģņØś ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ ĻĘĖ ļ»╝Ļ░ÉļÅäņÖĆ ĒŖ╣ņØ┤ļÅäļź╝ Ļ░üĻ░ü 63~71%, 50~78%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż[13,16,17].
MaheshwariņÖĆ Mukherji [18]ļŖö ĻĘĖļōżņØś ņ”ØļĪĆ ļ│┤Ļ│ĀņŚÉņä£ MRI ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ļŖö ņ¦äņŻ╝ņóģĻ│╝ ņ£ĪņĢäņóģņØä Ļ░Éļ│äĒĢĀ ņłś ņ׳ņØīņØä ĻĖ░ņłĀĒĢśņśĆļŗż. ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ļŖö ņĪ░ņ¦üņŚÉņä£ņØś ļ¼╝ņØś ļČäņ×É ĒÖĢņé░(molecular diffusion)ņŚÉ ļīĆĒĢ£ ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢśņŚ¼ ņ¦äņŻ╝ņóģņŚÉ ņ׳ņ¢┤ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ ļéśĒāĆļé┤ļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż[19]. ņØ┤ļź╝ ĒÖ£ņÜ®ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ Aikele ļō▒[20]ņØĆ single-shot spin-echo echo planar pulse sequenceļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņ¢╗ņØĆ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ ņłśņłĀĒøä ļ░£ņāØĒĢ£ ņ¦äņŻ╝ņóģ ņ¦äļŗ©ņØś ļ»╝Ļ░ÉļÅäņÖĆ ĒŖ╣ņØ┤ļÅä, ņ¢æņä▒ņśłņĖĪļźĀĻ│╝ ņØīņä▒ ņśłņĖĪļźĀņØä Ļ░üĻ░ü 77%, 100%, 100%, 75%ļĪ£ ļ│┤Ļ│ĀĒĢśņśĆļŗż.
ņĄ£ĻĘ╝ņŚÉļŖö ņ¦äņŻ╝ņóģņØś ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ non-echo planar imageņŚÉ ĻĖ░ļ░śņØä ļæö ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØ┤ Ļ░£ļ░£ļÉśņ¢┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ£╝ļ®░ ļīĆĒæ£ņĀüņ£╝ļĪ£ Half Fourier Acquisition Single Shot Turbo Spin Echo(HASTE; Siemens, Erlanagen, Germany) ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüĻ│╝ K-space sampling ļ░®ļ▓ĢņØä ņé¼ņÜ®ĒĢśļŖö BLADE(Siemens) ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüĻ│╝ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāü(General Electric)ņØä ļōż ņłś ņ׳ļŗż[21-24]. ĻĘĖ ņżæ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØĆ ņĄ£ĻĘ╝ ĻĘĖ ņ×äņāüņĀü ņ£ĀņÜ®ņä▒ņŚÉ ļīĆĒĢ£ ļ¦ÄņØĆ ņŚ░ĻĄ¼Ļ░Ć ņØ┤ļŻ©ņ¢┤ņ¦ĆĻ│Ā ņ׳ļŗż. ĒŖ╣Ē׳ ņłśņÜöĻ░Ć ņĀÉņĀÉ ļŖśņ¢┤ļéśĻ│Ā ņ׳ļŖö Ļ│Āņ×Éņן MRIņØś Ļ▓ĮņÜ░ susceptibility artifactņØś ņśüĒ¢źņØä ļŹö Ēü¼Ļ▓ī ļ░øļŖö ļ¼ĖņĀ£ņĀÉ ļĢīļ¼ĖņŚÉ ĻĖ░ņĪ┤ņØś ņŚÉņĮö ĒÅēļ®┤ ņśüņāüĻ│╝ Ļ░ÖņØĆ pulse sequenceņØś Ļ▓ĮņÜ░ artifactļĪ£ ņØĖĒĢ£ ņśüņāüņĀĢļ│┤ ņåīņŗżņØĆ 1.5TņŚÉ ļ╣äĒĢ┤ ļ│┤ļŗż ļŹö Ēü¼Ļ▓ī ļéśĒāĆļé£ļŗż. ņØ┤ļ¤¼ĒĢ£ Ļ▓ĮņÜ░ņŚÉ ņ׳ņ¢┤ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØĆ artifactņØś ņśüĒ¢źņØä ļŹ£ ļ░øĻĖ░ ļĢīļ¼ĖņŚÉ Ļ│Āņ×Éņן(3.0T)ņŚÉņä£ ļ│┤ļŗż ņ£ĀņÜ®ĒĢśĻ▓ī ņØ┤ņÜ®ļÉĀ ņłś ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż[25]. ĻĘĖļ¤¼ļéś ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØĆ ņČĢļ®┤(axial plane)ņØś ņśüņāüļ¦ī ņĀ£Ļ│ĄļÉśĻ│Ā, ņŻ╝ļ│Ć ļ╝łņØś ĻĄ¼ņĪ░Ļ░Ć ņל Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖļŖö MRIņØś ĒŖ╣ņä▒ņāü ņżæņØ┤ņÖĆ ņ£Āņ¢æļÅÖņŚÉ ņ׳ļŖö ņ¦äņŻ╝ņóģņØś ņĀĢĒÖĢĒĢ£ ņ£äņ╣śļź╝ Ļ┤Ćņ░░ĒĢśĻĖ░ņŚÉļŖö ĒĢ£Ļ│äĻ░Ć ņ׳ņ¢┤ TBCTņÖĆ ĒĢ©Ļ╗ś ņé¼ņÜ®ļÉśņ¢┤ņĢ╝ ĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż[26].
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņØä ņØ┤ņÜ®ĒĢśņśĆņØä Ļ▓ĮņÜ░ ļ¦īņä▒ ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņØś ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ ļ»╝Ļ░ÉļÅä, ĒŖ╣ņØ┤ļÅä, ņ¢æņä▒ ņśłņĖĪļźĀ, ņØīņä▒ ņśłņĖĪļźĀņØ┤ Ļ░üĻ░ü 94.1%, 100%, 100%, 83.2%ļĪ£ ļ│┤Ļ│ĀļÉśņ¢┤ ĻĘĖ ĒÜ©ņÜ®ņä▒ņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż.
ņ£äņØīņä▒ņØä ļ│┤ņØĖ 3ņśłņØś Ļ▓ĮņÜ░ ņłśņłĀ ņåīĻ▓¼ņāü 3 mm ļ»Ėļ¦īņØś ņ×æņØĆ ļ│æļ│ĆņØ┤ņŚłņ£╝ļ®░ ņśüņāüņØś Ļ░äĻ▓®(3 mm)ņ£╝ļĪ£ ņØĖĒĢśņŚ¼ ņ¦äņŻ╝ņóģņØ┤ ĒÖĢņØĖļÉśņ¦Ć ņĢŖņĢśņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż. ĻĘĖļ”¼Ļ│Ā ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļŖö ņ¦äņŻ╝ņóģ ĻĖ░ņ¦łņØś Ļ░üņ¦ł(keratin)ņØä ļ░śņśüĒĢśļŖö Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉśļ®░ Ļ░Ćņןņ×Éļ”¼ņØś Ļ│ĀĻ░ĢļÅä ņŗĀĒśĖĻ░Ć Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ņŚÉļŖö ļé┤ļČĆņØś ņĀĆņØīņśüņØĆ ņ¦äņŻ╝ņóģņØś ņŗżņ¦łĻ│╝ļŖö ļŗżļźĖ ņŚ╝ņ”Øņä▒ ļ│ĆĒÖöĻ░Ć ņĪ┤ņ×¼ĒĢ©ņØä ņłĀĒøä ņĪ░ņ¦ü Ļ▓Ćņé¼ļź╝ ĒåĄĒĢ┤ ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż.
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņłśņłĀĒøä ņ×¼ļ░£ĒĢ£ ņ¦äņŻ╝ņóģņØĆ 6ņśłĻ░Ć ņ׳ņŚłņ£╝ļ®░, 6ņśł ļ¬©ļæÉ ĒöäļĪ£ĒÄĀļ¤¼ ĒÖĢņé░Ļ░ĢņĪ░ņśüņāüņŚÉņä£ Ļ│ĀĻ░ĢļÅäņØś ņŗĀĒśĖļź╝ Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņ¢┤ 100%ņØś ļ»╝Ļ░ÉļÅäļź╝ ļ│┤ņśĆļŗż.
ņØ┤ļ▓ł ņŚ░ĻĄ¼ņØś ĒĢ£Ļ│äņĀÉņ£╝ļĪ£ļŖö ļ╣äņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ ĒÖśņ×ÉĻĄ░ņØ┤ 16ņśłļĪ£ 51ņśłņØś ņ¦äņŻ╝ņóģņä▒ ņżæņØ┤ņŚ╝ņŚÉ ļ╣äĒĢ┤ ņĀüņØĆ Ļ▓āņØä ļōż ņłś ņ׳Ļ▓Āļŗż. ļö░ļØ╝ņä£ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö ņ£äņ¢æņä▒ ņåīĻ▓¼ņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļŖö Ē¢źĒøä ļŹö ļ¦ÄņØĆ ĒÖśņ×ÉĻĄ░ņŚÉņä£ ņØ┤ļŻ©ņ¢┤ņĀĖņĢ╝ ĒĢĀ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉśļ®░, ņ×¼ļ░£ņä▒ Ēś╣ņØĆ ņ×öļźśņä▒ ņ¦äņŻ╝ņóģņŚÉ ņ׳ņ¢┤ņä£ļÅä ņČöĻ░ĆņĀüņØĖ ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢĀ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉ£ļŗż.