비외상성 시신경병증에서 내시경적 비내 시신경감압술 3예
Three Cases of Endoscopic Endonasal Optic Nerve Decompression for Nontraumatic Optic Neuropathy
Article information
Trans Abstract
The rate of traumatic or nontraumatic optic neuropathy has increased in recent decades. High dose steroid, surgery and combined treatment are used for management of optic neuropathy. Surgical intervention using an endoscopic intranasal approach is expected to provide a safe and effective method for optic nerve decompression. We present outcomes of three patients with neuropathy who underwent endoscopic optic nerve decompression. Of the three patients, two showed improvement: from hand motion to 0.8 and 0.63, respectively. However, one patient who was not able to perceive light did not improve vision after surgery. The difference between the recovered patients and the patient who did not show improvement may be a result of initial visual acuity. Early diagnosis and prompt surgical management could increase the likelihood of improved visual performance; however, this may be limited to patients whose initial visual acuity is better than light perception.
서 론
외상성 시신경병증은 사고로 인한 안면 외상에서 약 2~5%로 발생된다고 보고되고 있으며 시신경관의 직접 골절, 신경내부종, 혈종, 미세혈관의 전단 손상 등의 다양한 기전에 의한다[1,2]. 반면 비외상성 시신경병증은 외상성 시신경병증에 비하여 상대적으로 드물게 보고되고 있으며, 종양이나 감염, 골이형성증 등의 병적 조건에서 시신경이 압박되어 이차적으로 발생하는 것으로 알려져 있다[3].
급성 시신경병증에서 치료는 경과 관찰, 고용량 스테로이드 요법, 시신경감압술, 병합요법 등이 고려되고 있다[4]. 하지만 Cochrane 데이터베이스에 따르면 외상성 시신경병증에서 부신피질호르몬 치료 및 수술적 치료에 대해서는 무작위 대조시험이 이루어진 바가 없어 아직 치료에 합의가 도출되지 않았다[5]. 문헌들에 따르면, 아무런 치료 없이 경과 관찰만 한 경우 20~38%가량의 시력 회복을 보이기도 하였고[4,6], 초기 시력에 따라 보존적 치료만 시행한 증례에서도 고용량 스테로이드 또는 수술적 감압술을 시행하였을 때와 유사한 정도의 시력 회복을 보이기도 하였으며[4,7], 환자의 상황에 따라 고용량 스테로이드 치료를 신중히 결정해야 할 수 있기에[8], 임상의들은 다양한 치료방법과 그에 따라 예상되는 이득과 손실에 대해 환자와 면밀하게 상의 후 사전 동의를 구해 치료에 임해야 한다.
시신경병증에서 수술적 치료에 대해서는 시력과 관련하여 수술의 적응증 및 수술 시기에 따라서 술자마다 의견이 다양하다. 시력이 0.02 이하인 경우 눈앞 30 cm에서 손가락을 셀 수 있는 시력을 안전수지, 눈앞에서 물체가 움직이는 것을 감지할 수 있는 시력을 안전수동, 눈앞에서 불빛을 감지할 수 있는 시력을 광각인지로 표기하게 된다. 여러 연구들을 통하여 보았을 때 외상성 시신경병증에서 치료 전 광각인지가 안되는 환자에 비해 광각인지 이상의 시력을 보이는 환자에서 술 후 시력이 호전될 확률이 높다고 보고되고 있다[4,9,10,11]. 이에 저자들은 비외상성 시신경병증에서도 외상성 시신경병증의 경우와 같이 치료 전 시력이 환자의 예후에 영향을 미칠 것으로 보고, 비외상성 시신경병증에서 시행한 시신경감압술을 3예를 문헌 고찰과 함께 보고하고자 한다.
증 례
증례 1
57세 여자 환자가 14일 전부터 시작된 우안의 시력 저하 및 두통을 주소로 타병원 내원, 시행한 검사에서 우측 시신경 주위 종양 소견으로 전원되었다. 이학적 검사에서 환자는 내원 11일 전부터 광각인지가 불가능하였고, 우안의 상대적구심성동공운동장애 양성 소견을 보였다. 혈액검사에서 백혈구, 적혈구 및 혈소판 수치를 포함한 모든 수치는 정상이었다.
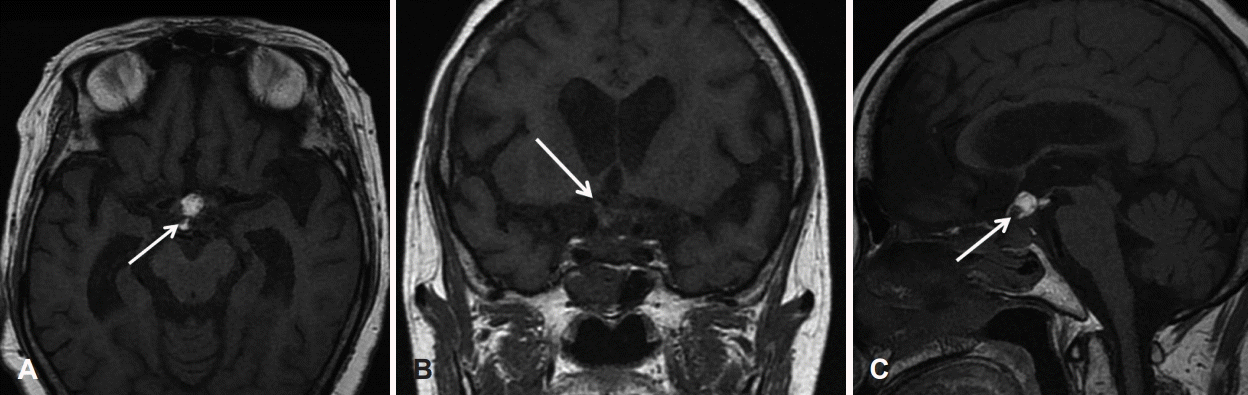
안와 자기공명영상에서 1.6×0.8×1.0 cm 크기의 낭성 종괴가 함기화된 우측 앞침상돌기에 위치하여 시신경을 상외측에서 내하측으로 압박하는 소견이 확인되었는데, T2 강조영상에서 현저한 고신호 음영을 보이고, gadolinium 조영제 투여 후 T1 강조 영상에서 모두 불규칙적인 고신호 음영을 보였다. 그 밖에 인접한 뇌나 안와내의 병변은 관찰되지 않았다(Fig. 1).

Initial Orbit MRI showing 1.6×0.8×1.0 cm sized cystic lesion with an heterogenously increased signal intensity at pneumatized right anterior clinoid process (white arrows) compressing right optic nerve (white line). T1-weighted image. Axial scan (A). Coronal scan (B). Sagittal scan (C).
환자는 우측 앞침상돌기에서 기원하는 점액낭종 진단 하에 내시경하 경사골동 경접형동 접근법으로 점액낭종을 확인 후 제거술 및 안와개방술을 시행하였다. 수술 후 낭종으로부터 채취한 조직표본에서 점액낭종으로 확진되었다. 수술 후에 환자의 두통은 소실되었고, 5일간의 정맥 항생제 flomoxef, metronidazole, isepamicin과 경구 스테로이드 methylprednisolone 24 mg BID 5일간, 이후 5일간 감량하여 10일 투여하였으나 술 후 3개월까지 환자의 안증상은 호전되지 않았다.
증례 2
78세 여자 환자가 2개월 전부터 서서히 진행되는 양측 시력 저하를 주소로 타병원 내원, 시행한 자기공명영상에서 두개인두종 의증으로 본원으로 전원되었다. 본원 내원 시 이학적 검사에서 환자는 양안 시력 안전수동이며, 양측 동공 고정으로 상대적구심성동공운동장애 측정이 불가능하였다. 혈액검사에서 백혈구, 적혈구 및 혈소판 수치는 정상이었으며, 만성콩팥기능상실로 혈중요소질소 및 크레아티닌 수치가 증가되어 있었다.
안장 자기공명영상에서 안장 위 공간에 제3 뇌실까지 연장되어 있는 2.1×2.5×3.2 cm 크기의 낭성 종괴 소견이 관찰되었는데, T1 강조 영상에서 다소 증가된 신호, T2 강조 영상에서 고신호강도 소견을 보였다(Fig. 2).

Initial Sella MRI showing 2.1×2.5×3.2 cm sized, mild increased signal intensity at T1, cystic mass lesion (white arrows) in the suprasellar area, extension to 3rd ventricle. T1-weighted image. Axial scan (A). Coronal scan (B). Sagittal scan (C).
환자는 두개인두종 의증 및 이로 인한 양측 시신경병증 진단 하에 내시경하 경비중격 경접형동 접근법으로 내시경적 조대술 및 시신경감압술을 시행하였다. 수술 후 종괴로부터 채취한 조직표본에서 두개인두종으로 진단되었다. 수술 후에 환자는 정맥 항생제 ceftriaxone 및 3일간의 정맥 스테로이드 hydrocortisone 50 mg TID와 20일간의 경구 스테로이드 prednisolone 7.5 mg QD를 투여하였다. 수술 10병일 째 환자는 우안 0.8, 좌안 안전수지 50 cm까지 시력 회복 및 양안의 전반적인 시야 회복을 보였다(Fig. 3). 수술 1년 후 추적을 위해 촬영한 안장 자기공명영상에서 안장 위 공간에 1.4×1.7×1.3 cm 크기의 수술 후 변화 소견만을 보였다(Fig. 4).

Visual field change. Preoperative Humphrey visual field test shows total visual field defect in both eyes (A). 10 days after surgery, visual field recovers at temporal side in both eyes, especially in the left eye (B).
증례 3
66세 여자 환자가 16일 전부터 시작된 좌안의 아래쪽 시력 저하를 주소로 타병원 내원, 시행한 검사에서 좌측 접형사골봉소(Onodi) 주위 종양 소견으로 전원되었다. 이학적 검사에서 환자는 내원 13일 전부터 광각검사에 반응을 보이지 않았으나 내원 하루 전부터 광각인지가 가능하기 시작하였으며, 위쪽 시야에서 제한적으로 안전 수동이 가능하였다. 좌안의 상대적구심성동공운동장애는 양성 소견을 보였다. 혈액검사에서 백혈구, 적혈구 및 혈소판 수치를 포함한 모든 수치는 정상이었다.
부비동 자기공명영상에서 좌측 접형사골봉소에 골미란을 동반한 1.8×1.1×0.8 cm 크기의 낭성 종괴가 관찰되었는데, T2 강조 영상에서 현저한 고신호 음영을 보이며 좌측 시신경관을 둘러싸고 압박하는 소견을 보였다(Fig. 5). 그 외에 양측 상악동, 사골동, 접형동의 점막골막 비후를 동반하였다.

Initial paranasal sinus MRI showing 1.8×1.1×0.8 cm sized cystic lesion with an heterogenously increased signal intensity of left sphenoethmoidal (Onodi) cell with bony erosion (white arrows) encirculing and compressing the left optic nerve (canal). T2-weighted image. Axial scan (A). Coronal scan (B). Sagittal scan (C).
내시경하 경사골동 경접형동 접근법으로 낭종의 감압술을 시행하였다. 낭종으로부터 채취한 조직표본에서 점액낭종으로 최종 진단되었다. 수술 후 5일간의 정맥 항생제 flomoxef, metronidazole, isepamicin과 정맥 스테로이드 methylprednisolone 250 mg QID 3일, 이후 경구 스테로이드 prednisolone을 1주씩 6 0, 5 0, 4 0, 3 0 m g으로 감량하여 총 4주간 더 유지하였다. 수술 1병일 째 환자는 50 cm 거리에서 안전수지가 가능한 정도까지 시력이 회복되었다. 수술 5병일째에는 좌안 시력 0.63까지 회복되었고, 상대적구심성동공운동장애 음성 소견을 보였으나 아래쪽 시야 결손은 지속되었다(Fig. 6B). 수술 5주 후에는 좌안 아래쪽 시야 역시 부분적으로 회복되었다(Fig. 6C).

Visual field change. Preoperative Humphrey visual field test shows total visual field defect in the left eye (A). 5 days after surgery, visual field mildly recovers in superonasal area in the left eye (B). 5 weeks after surgery, the visual field recovers progressively in whole areas in the left eye (C).
고 찰
외상성 시신경손상 환자의 적절한 치료에 대해서는 아직까지도 다양한 의견이 있으나, 대부분의 환자에서는 경과 관찰만으로는 자연회복을 기대하기 어려워 시력 회복의 가능성을 증가시키기 위해 고용량 스테로이드 요법, 시신경감압술 또는 병합요법에 대해 고려하게 된다. 하지만 무작위 대조시험이 이루어지지 않았기에, 수술적 중재를 시행한 외상성 시신경손상에서 시력 회복이 자발적 회복으로 인한 것인지, 또는 중재의 효과인지는 불분명한 경우가 많다. 아직 논란이 있지만, 후향적 증례 고찰을 통해 일반적으로 치료 전 광각인지가 안 되는 환자에 비해 광각인지 이상의 시력을 보이는 환자에서 시력이 호전될 확률이 높다고 생각되고 있다[4,9-11]. 2016년 Dhaliwal 등[12]이 발표한 체계적 문헌 고찰에 따르면, 외상성 시신경병증에서 시신경감압술을 3일 이내에 시행하였을 때 57%에서, 7일 이후에 시행하였을 때 51%에서 회복을 보여 수술 시기에 따른 회복률에는 큰 차이가 없음을 알 수 있었다. 반면 술 전 광각인지가 안 되는 환자들은 41%에서 회복함으로, 술 전 광각인지, 안전수동, 안전수지가 가능한 환자군에서 각각 89, 93, 85%의 회복률을 보였다.
비외상성 시신경병증은 상대적으로 드물며, 주로 갑상샘눈병증, 비부비동염 및 안와주위종양 등에 의해 발생하는 것으로 보고되고 있다[13]. 주로 만성 질환에 의한 것으로 외상에 의한 경우와 달리 시력의 자발 회복을 기대하기 어렵기 때문에, 병리적 원인에 대한 수술적 교정이 가능하다면 시신경감압술을 고려해야 한다[3,13]. 비외상성 시신경병증에서 시신경 감압술을 시행하여 시력이 회복됨을 확인하여 시신경감압술의 치료 효과를 확인할 수 있었으며, 술 후 시력 회복은 37.5~80.0% 정도로 보고되고 있다[13-16]. 시신경감압술에서 경비강 내시경적 접근법은 비교적 적은 이환율을 가지며 안와꼭지와 시신경관을 잘 확인할 수 있는 방법이나, 일반적으로 접형동과 인접해 있는 시신경의 아래 안쪽 부위에 제한적으로 시야가 확보된다는 단점이 있다[3].
본 연구에서는 비외상성 시신경병증 3례에 대해 내시경적 시신경감압술을 시행 후 고용량 스테로이드 치료를 시행하였다. 첫 번째 증례에서는 갑작스레 발생한 전맹 11일째 시신경감압술을 시행하였고, 치료 전 광각에 반응을 보이지 않았기에 시력의 회복을 보이지 않았다. 두 번째 증례에서는 두개인두종으로 인한 양안의 시력 손상이 2개월간 서서히 진행되었으나 양안 안전수동이 가능할 때 시신경감압술을 시행하였으며, 이후 스테로이드 치료를 하여 우안 0.8, 좌안 안전수지 50 cm까지 시력이 회복되었다. 세 번째 증례에서는 접형사골봉소의 점액낭종으로 인해 광각반응이 되지 않는 시력 손상이 발생하였으나 12일 경과 후 자발적으로 시력이 광각반응을 보이는 정도까지 회복되었으며, 이후 24시간 이내에 시신경감압술과 스테로이드 치료를 시행하여 극적인 증상 호전을 볼 수 있었다.
첫 번째 증례와 같은 앞침상돌기에 발생하는 점액낭종의 경우 국외 학술지에도 극히 드물게 보고되고 있으나, 비외상성 시신경병증의 치료에 대한 예후를 고찰하기에 좋다고 생각한다. 2014년까지 국외 학술지에 총 16예가 보고되었으며, 수술적 감압술을 시행한 경우에서는 광각검사에 반응을 보이지 않는 경우 1예에서만 술 후 시력 회복을 보이지 않았다[17]. 종양에 의한 비외상성 시신경병증의 경우 종양의 직접적 종괴 효과에 의한 시신경 손상 또는 종양에 의한 혈관폐색으로 발생하는 시신경의 부종이나 창백이 그 원인이 될 수 있다[18,19]. 저자들은 광각검사에 반응하지 않은 경우 상기 기전으로 인한 시신경 손상이 비가역적인 단계까지 진행되었을 것이라 생각한다. 시력이 회복된 두 증례의 환자들에서 점진적인 시력 손실이 발생하였던 것과 달리, 첫 번째 증례의 환자는 갑작스러운 전맹이 발생하였던 점도 비가역적 시신경 손상과 유의미한 연관이 있을 것으로 추정된다.
급성 비외상성 시신경병증에서 아직 치료적 합의가 도출되지 않았기에, 각 증례 환자마다 유사한 문헌과 경험을 토대로 수술적 및 스테로이드 치료를 시행하였다. 이에 각 증례에서 사용한 스테로이드 약제의 종류와 용법, 용량, 기간이 모두 상이하여 예후의 차이를 보였을 가능성이 있다. 하지만 본 증례들에서는 안와와 시신경 주위에 발생한 종양이 원인이었다는 점에서 스테로이드 치료보다는 수술적 감압술이 예후에 훨씬 중요한 역할을 하였을 것이라 생각된다. 비외상성 시신경병증 중에서도 갑상샘눈병증이나 종양을 동반하지 않은 단순 비부비동염 등이 원인일 경우 종괴 효과의 영향이 비교적 적어 약물치료가 더 크게 기여할 수 있을 것으로 보인다. 따라서 비외상성 시신경병증에서도 원인 질환에 따라 적절한 치료와 예후가 상이하게 나타날 가능성이 있어 추가적인 보고가 필요할 것으로 생각된다.
시신경감압술의 시기에 대해서는 많은 논의가 있어 왔으나 최근의 문헌들에 따르면 외상성 시신경병증에서 수술 시기보다 술 전 광각반응을 보이는지 여부가 예후에 중요한 것으로 생각된다[4,9-12]. 저자들은 본 증례 및 문헌 고찰을 통해, 비외상성 시신경병증도 외상성 시신경병증과 마찬가지로 수술 전 환자의 시력이 광각반응이 소실되기 전에 이른 시신경감압술을 시행할 경우 시력 회복의 가능성이 높음을 확인하였다. 또한 비외상성 시신경병증에서는 일반적으로 서서히 시력이 악화되는 경과를 보이며 안증상의 자발 회복을 기대하기 어려워 외상성 시신경병증에 비해 시신경감압술을 더욱 적극적으로 고려해야 함을 확인하였다. 따라서 비외상성 시신경병증에서 시력 손상이 나타난 후부터 상당한 시간이 경과되었다 하더라도, 수술 전 정밀한 안과적 검사 후 시신경병증에 대한 수술적 교정이 가능하다면 가급적 적극적으로 감압술을 시행하여 안증상의 개선을 도모해야 할 것이다.