경성 경구강 내시경을 이용한 게실 절개술 후 재발로 개방 게실 절제술을 시행한 젠커게실 1예
A Case of Zenker’s Diverticulum Who Underwent Secondary Open Diverticulectomy After Failed Rigid Transoral Endoscopic Diverticulotomy
Article information
Trans Abstract
The traditional approach to diagnosis and management of Zenker’s diverticulum is open surgical treatment. More recently, however, endoscopic technique is also frequently used for Zenker’s diverticulum because it has advantages of shortening operation time, postoperative hospitalization and reducing the complication such as recurrent laryngeal nerve injury. A 75-year-old male, who was diagnosed with Zenker’s diverticulum, underwent a secondary open diverticulectomy after failed attempt at rigid transoral endoscopic diverticulotomy. Here we report this case with a review of literature.
서 론
젠커(Zenker)게실은 해부학적 결손이나 연하곤란으로 인해 인두부 점막이 후방으로 돌출되어 발생하며 Killian’s triangle이라고 불리는 윤상인두근(cricopharyngeus muscle)과 하인두수축근(inferior pharyngeal constrictor muscle) 사이에서 주로 발생한다[1].
대부분의 환자는 무증상으로 치료가 필요하지 않지만 게실의 크기가 큰 경우 음식물의 역류, 흡인으로 인한 기침, 질식, 인두 이물감 등의 증상이나 흡인성 폐렴 등의 합병증이 나타날 수 있다[2]. 이 중 연하곤란이 가장 흔한 증상으로 알려져 있으며, 이러한 증상들이 발생하면 치료가 필요하고 일반적으로 수술이 원칙이다[3].
젠커게실에 대한 치료에는 개방적 접근법, 경직성 경구강 내시경 또는 연성 내시경을 이용한 접근법을 포함한 여러 방법이 있다[4]. 젠커게실에 대한 표준치료는 윤상인두근 절개술, 개방 게실 절제술 등과 같은 개방적인 외과적 술식이었으나, 최근 내시경적 접근을 통해 수술 시간 및 입원기간을 단축시킬 수 있고 환자의 경구 섭취를 더 빠르게 재개할 수 있으며, 반회후두신경 손상과 같은 전반적인 합병증 발생이 적다고 보고되고 있어 많이 이용되고 있다[5].
본 저자들은 젠커게실에 대한 일차 치료로 경성 경구강 내시경을 이용한 게실 절개술을 시행한 이후 삼킴곤란 증상의 호전이 있었으나 경과 관찰 중 음식물 역류 및 연하곤란 악화를 보이는 재발 환자에게 이차 개방 게실 절제술을 시행하여 호전된 증례를 경험하여 문헌 고찰과 함께 보고하고자 한다.
증 례
환자는 75세 남자로 삼킴곤란을 주소로 2006년 5월 본원 소화기내과에 내원하였다. 환자는 과거력 및 가족력에서 특이 소견이 없었으며 경부 외상 및 수술력 또한 없었다.
2006년 5월 본원에서 시행한 위내시경상 게실은 후인두 직하방에서 관찰되었고(Fig. 1A), 상부식도조임근(upper esophageal sphincter)은 그 앞쪽으로 관찰되었다. 2006년 5월 본원에서 시행한 식도조영술상에서 조영제가 채워진 6×3 cm 크기의 돌출된 식도낭이 인두식도분절의 후벽에서 관찰되었다. 이 식도낭에 의해 경부식도는 부드러운 외부 압력을 받고 있었지만 내용물을 삼킬 때 조영제는 잘 통과하였다. 상기 환자는 본원에서 위내시경 및 식도조영술 시행 후 젠커게실 진단하 본원 추적 관찰 중이었다.
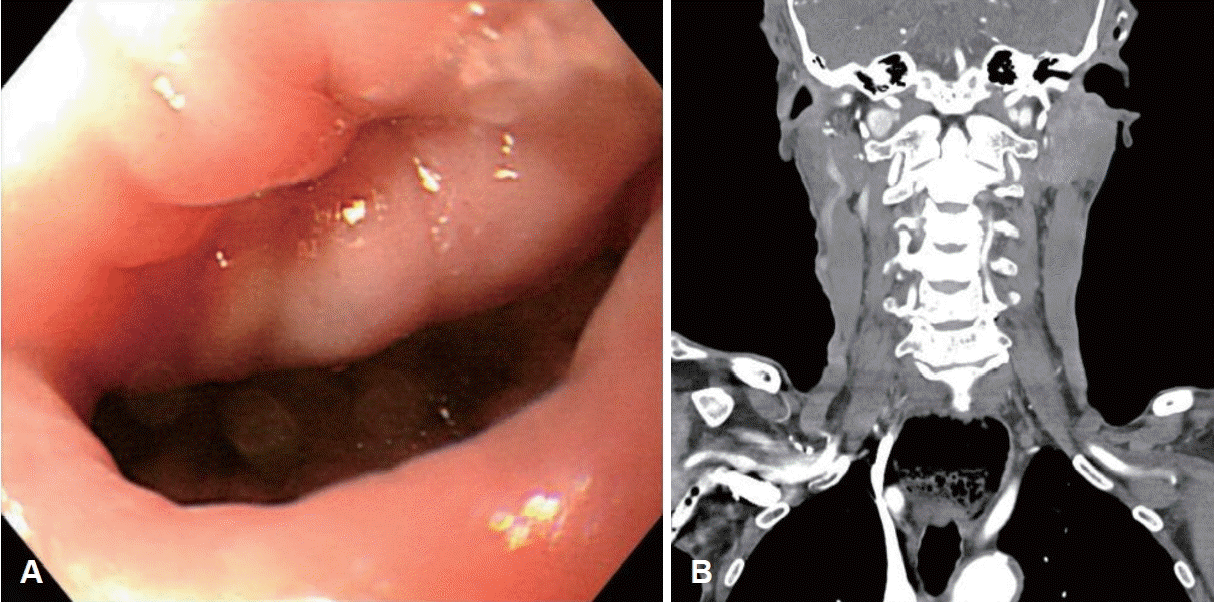
Preoperative esophagoscopy and CT image. A: The gastroscopy reveals that the diverticulum was observed just below the posterior pharynx, and upper esophageal sphincter was observed anteriorly. B: Post-contrast CT scan shows 5.5×3.0 cm sized sac with air and liquid contents behind the esophagus was confirmed in pharyngo-esophageal junction.
환자는 2018년 1월 구취와 역류 증상이 악화되어 본원 이비인후과를 내원하였고 후두경상 후인두낭의 음식물 저류가 관찰되었다. 2018년 1월 시행한 경부 전산화단층촬영 결과 인두식도 접합부에 경부 식도 뒤쪽으로 5.5×3 cm 크기의 공기와 액체를 포함한 낭이 관찰되었다(Fig. 1B).
증상 개선을 위해 우선 1차 치료로 내시경 게실 절개술을 계획했다. 수술은 전신마취하에 시행하였으며 현수 후두경(suspension laryngoscope)으로 식도를 노출시킨 후 게실 및 상부식도조임근을 확인하였다. 이후 게실 내 이물질을 제거한 후 게실의 길이를 확인했으며 게실과 식도 사이의 공동벽 양측에 봉합사를 통해 고정시켜 양측으로 장력을 가하였다. 45 mm 위장관 자동 스테이플러(gastrointestinal autostapler)를 사용하여 공동벽을 절개하였고, 공동벽 하방의 절개가 불충분한 부분은 전기 소작기를 이용하여 게실의 전벽 끝부분까지 박리하고 수술을 마쳤다(Fig. 2A).
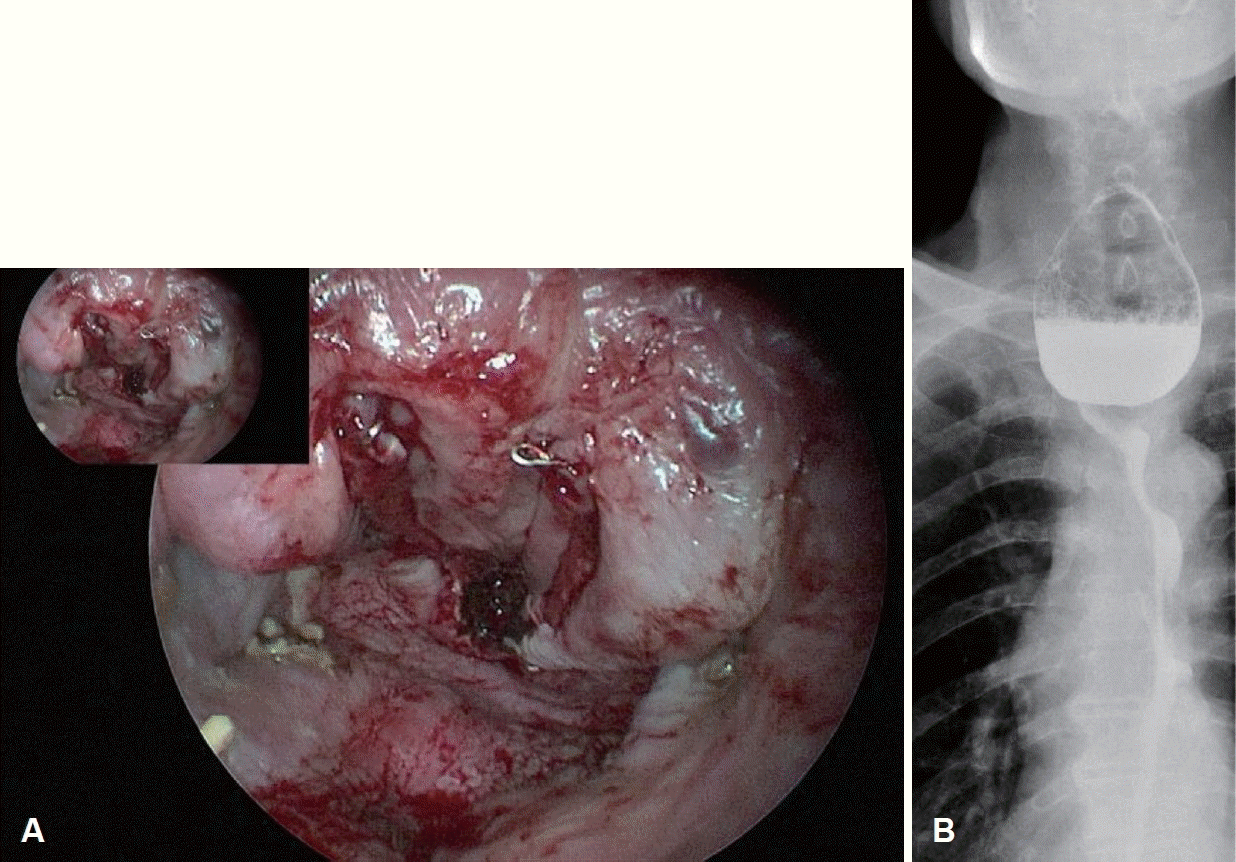
Rigid transoral endoscopic diverticulotomy (1st operation). A: Anterior wall of diverticulum was divided by endo-gastrointestinal autostapler and monopolar dissection. B: Even though postoperative esophagography showed no evidence of leakage, the contrast agent was concentrated in the lower part of the diverticulum.
술후 1일째에 시행한 식도조영술상에서 조영제를 삼켰을 때 게실 절개술 시행 부위로 조영제가 채워진 것이 관찰되었으나 조영제 누출이나 누공 소견은 보이지 않았다(Fig. 2B). 또한 경부 전산화단층촬영을 시행하였고, 게실 절개술 시행 부위로 조영제가 채워진 게실이 일부 남아있으나 크기가 작아졌고, 마찬가지로 조영제 누출이나 누공 소견은 보이지 않았다. 상기 환자는 게실의 크기가 줄어들고 누공이 없는 것을 확인한 후 식사를 시작하였고, 후두경상 게실 아래쪽 일부 음식물이 남아 있는 소견이 보이나 역류 및 구취 증상이 호전되었으며 술후 4일째 퇴원하였다.
술후 2년째 추적 관찰 중이며 역류증상은 호전되었으나 지속적인 수분 섭식장애를 호소하고 있었고, 이에 대해 재발방지를 위한 개방 게실 절제술과 윤상인두근 절개술을 추가적으로 계획하였다. 수술은 전신마취하에 시행하였으며 좌측 경부 접근법(left cervical approach)을 시도하였다. 흉쇄유돌근의 전연을 따라 피부 절개를 시행하였고 견갑설골근(omohyoid muscle) 및 목신경고리(ansa cervicalis)를 절제하였다. 수술중 반회후두신경을 확인한 후 보존하였고, 식도벽에서 게실을 박리하여 이전 수술에서 사용된 stapler를 확인하였고, 봉합 부위를 따라 60 mm 위장관 자동 스테이플러를 사용하여 게실을 절제했다(Fig. 3A and B). 이후 주변 근육들을 봉합하여 제거된 부위를 보강 및 내번시킨 후 윤상인두근 절개술을 시행하였다.
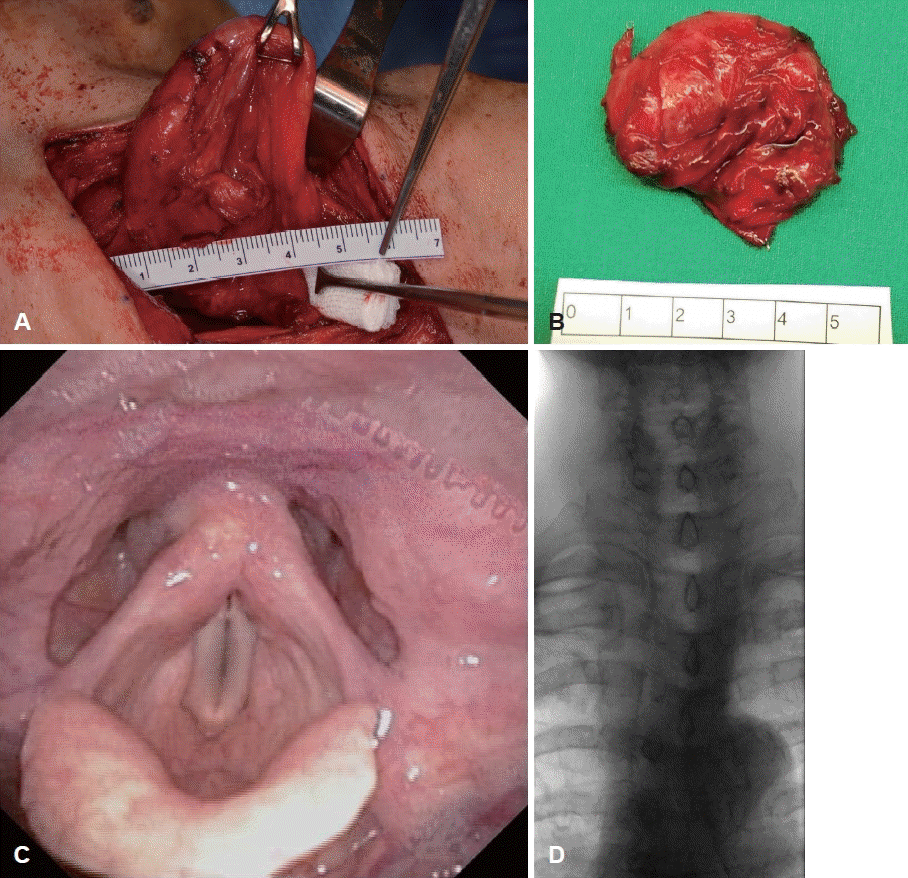
Open diverticulectomy for refractory Zenker’s diverticulum. A: The stapler used in the previous operation was confirmed by dissecting the diverticulum from the wall of the esophagus. B: Open diverticulectomy (2nd operation) specimen. C: After 2 weeks, laryngoscopy shows transient left vocal cord paresis, but vocal cord mobility is observed. D: After 1 year, esophagography showed no evidence of contrast leakage nor fistula in cervical esophagus.
술후 일시적으로 발생했던 편측 성대 마비는 술후 3개월째에 호전되었다(Fig. 3C). 수술 후 4개월과 1년째 추적 식도혈관조영술을 시행하였고, 젠커게실은 소실된 상태이고 조영제 누출은 관찰되지 않았으며, 수술 후 2년 뒤에도 증상의 재발 없이 외래 추적 관찰 중이다(Fig. 3D).
고 찰
젠커게실은 가성게실의 일종으로 게실의 벽은 점막과 점막하층으로 구성되어 있으며 주변근육 간의 작용에 의한 벽내 압력(intramural pressure)의 증가와 삼킴반사에 있어서 윤상인두근과 상부식도조임근의 불완전한 이완 작용의 결과로 게실이 점점 부풀어 오르게 된다[6-8]. 젠커게실의 외과적 치료는 피부절개를 통한 게실 절제술, 게실 고정술, 윤상인두근절제술, 아르곤이나 CO2 레이저를 이용한 내시경적 절제술, 내시경적 스테이플러를 사용한 게실 절제술 등 다양한 방법이 있다[4]. 경추 변형 또는 입벌림 장애가 동반되어 있을 경우 연성내시경을 이용한 게실 절개술을 고려할 수 있으며, 게실의 크기가 3 cm 미만인 경우 내시경적 접근이 선호된다[2]. 최근 젠커게실에 대한 내시경적 절제술이 많이 시도되고 있지만, 6 cm 이상의 중격을 가진 큰 젠커게실의 경우 내시경적 접근만으로는 중격을 완전히 제거할 수 없고 식도 내에 공동을 형성할 가능성이 커서 재발률이 높아 가급적이면 개방적 접근을 통해 절제해야 한다[9]. 특히 4 cm 이상(diverticulum grade III) 크기의 게실에 대해 내시경적 치료를 시행할 경우 술후 삼킴곤란 등의 증상이 재발할 가능성이 높은 것으로 나타났다[10].
본 증례에서 내시경 술식이 성공하지 못한 이유는 게실의 크기가 컸고, 게실 후방 벽이 아래쪽으로 내려가 있는 상태가 주요한 것으로 생각되고, 이는 내시경적 접근이 게실에 병치된 윤상인두근의 길이만큼만 절개가 가능하여 불완전한 근절개술의 가능성이 있고, 완전한 근절개술이 이뤄졌다 하더라도 잔류게실의 크기가 클 경우 여전히 음식을 삼킬 때 장애요인이 될 수 있다는 보고와 일치한다[11]. 한편, 게실의 크기가 너무 작아 내시경 진입이 불가능한 경우, 하악궁(mandible arch)의 너비가 2.5 cm 미만인 경우, 절치(incisor)에서 1 cm 이상의 피개교합(overbite)이 있는 함몰된 하악이 있는 경우, 절치에서 2.5 cm 이상의 크기로 입을 벌릴 수 없는 경우, C4-C7 경추 위치에서 2 cm 이상 경추 골극이 있는 경우 등의 환자의 해부학적 요인에 의해 내시경적 처치가 제한적이거나 불가능하여 외과적 처치가 필요한 경우도 있다[12]. 따라서 여러 가지 요인에 의해 내시경적 접근이 실패했을 경우 개방 게실절제술과 윤상인두근 절개술 시행을 고려할 수 있다[5].
젠커게실에 대한 1차 내시경적 치료에도 불구하고 연하곤란, 역류 등 게실로 인한 증상의 재발은 18.4% 정도로 보고되고 있다[6]. 증상의 정도는 functional oral intake scale을 이용하여 평가할 수 있고, 본 증례에서는 수술 후 역류는 호전되었으나, 수분 섭식 시 특별한 준비가 필요한 grade III로 수술적 처치가 고려되었고[13], 이러한 경우 전통적으로는 개방수술이 권장된다[14]. 본 증례와 같이 스테이플러를 사용한 내시경 접근법 이후에 증상 재발로 이차 개방 수술을 한 경우에 대해서는 다기관 연구에서 8예에서 시행하였다고 보고하고 있고, 게실의 크기는 1-5.5 cm였다[14]. 2차 수술로 내시경적 접근도 활용할 수 있으나, 게실의 점막 상태, 술자의 익숙함, 환자 요인 등을 고려하여 2차 수술법을 선택하여야 한다[14].
결론적으로, 역류와 연하곤란 증상이 없는 경우는 특별한 처치 없이 추적 관찰이 가능하나 증상을 유발하는 큰 젠커게실의 경우 이에 대한 처치가 필요하며[2], 난치성 중격 또는 잔류 게실은 술후 증상 재발 가능성이 있고, 개방 게실 절제술 시행 과정 중 반회후두신경에 대한 견인 손상으로 인해 일시적인 성대마비를 유발할 수 있다[15]. 젠커게실에 대한 여러 가지 치료 방법 중 최근 내시경적 처치가 높은 성공률을 보이고 있고 수술적 처치에 비해 덜 침습적이며, 굴곡형 내시경을 사용하여 시술하는 경우 전신마취가 필요 없어 입원기간이 짧고 신경손상 등의 합병증 발생이 적어 많이 선호되고 있다[3]. 하지만 본 증례와 같이 게실이 크고 내시경적 처치 후 증상이 재발한 경우에는 고식적인 개방 게실 절제술이 필요하며, 수술 시행 후에는 추후 재발 또는 누공 형성 여부를 확인하기 위해 주기적으로 내시경, 식도 조영술, 경부 컴퓨터단층촬영 등 영상 장치를 이용한 지속적인 추적 관찰이 필요하다.
본 증례는 젠커게실에 대한 일차 치료로 경성 경구강 내시경적 게실 절개술을 시행하였고 이후 재발하여 이차 개방 게실 절제술을 시행하였으며, 술후 반회후두신경 견인손상에 의한 일시적인 성대마비가 발생했으나 호전된 경과를 통해 수술 시 신경 손상에 대한 각별한 주의를 기울여야 하고, 이차 개방 게실 절제술을 통한 증상이 호전된 증례를 경험하여 이를 문헌 고찰과 함께 보고하는 바이다.
Acknowledgements
This study was supported by the Soonchunhyang University Research Fund.
Notes
Author Contribution
Conceptualization: Young Jeong Lee, Ki Nam Park. Formal analysis: Jeong Hyun Lee, Jun Yeong Jeong. Funding acquisition: Ki Nam Park. Project administration: Young Jeong Lee, Ki Nam Park. Supervision: Ki Nam Park. Visualization: Jeong Hyun Lee, Jun Yeong Jeong. Writing—original draft: Young Jeong Lee, Ki Nam Park. Writing—review & editing: Jeong Hyun Lee, Jun Yeong Jeong, Ki Nam Park.
