 |
 |
AbstractPerioperative stroke is one of the most fatal complications for patients as well as for doctors. It is defined as a brain infarction or hemorrhage, occurring during or within 30 days after a surgical procedure. Most of the perioperative strokes have ischemic etiology while only 1% has hemorrhagic etiology, according to one study. The incidence of perioperative stroke is influenced by the complexity and type of the surgery. Generally, its incidence is very low, being about to 0.1-1.9%, with majority of the cases pertaining to cardiac, vascular, neurological surgeries. Based on our research, most cases are perioperative strokes that occur after cardiac and vascular surgeries. Here we report two cases of cerebral infarction after endoscopic sinus surgery, which are very rare.
мДЬ л°†мИШмИ†кіА놮лЗМм°Єм§С(perioperative stroke)мЭілЮА мИШмИ† м§СмЭілВШ мИШмИ† нЫД л∞ЬмГЭнХЬ лЗМм°Єм§СмЭД лЬїнХШк≥† лМАлґАлґДмЭШ к≤љмЪ∞ нЧИнШИмД±мЭіл©∞, кЈЄм§СмЧРмДЬлПД мГЙм†Дм¶Э(embolism)мЭі мЫРмЭЄмЭі лРШлКФ к≤љмЪ∞к∞А к∞АмЮ• лІОлЛ§[1,2]. мИШмИ†кіА놮лЗМм°Єм§СмЭА л∞ЬмГЭ땆мЭі лВЃмІАлІМ, мИШмИ† нЫД мВђлІЭ땆 м¶Эк∞А, мЮђмЫР кЄ∞к∞ДмЭШ м¶Эк∞А, мЮ•мХ† л∞ЬмГЭ땆 м¶Эк∞А лУ± мЛђк∞БнХЬ к≤∞к≥Љл•Љ міИлЮШнХШкЄ∞ лХМлђЄмЧР мЭШмВђлУ§мЭі к∞АмЮ• лСР놧мЫМнХШлКФ нХ©л≥См¶Э м§С нХШлВШмЭілЛ§[1,3].
мЭЉл∞Шм†БмЭЄ мЩЄк≥ЉмИШмИ†мЧРмДЬмЭШ мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ땆мЭА лМАлЮµ 0.2~0.7%л°Ь лІ§мЪ∞ лВЃлЛ§[4]. нХШмІАлІМ лЗМм°Єм§СмЭШ к≥Љк±∞놕мЭі мЮИлКФ к≤љмЪ∞, к≤љлПЩлІ•нШСм∞©мЭі лПЩл∞ШлРЬ к≤љмЪ∞, мШИм†ХмИШмИ†(elective surgery)л≥ілЛ§лКФ мЭСкЄЙмИШмИ†(urgent surgery)мЭШ к≤љмЪ∞мЧР мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ땆мЭі лЖТмЭА к≤ГмЬЉл°Ь мХМ놧솪 мЮИлЛ§[1,3].
м†АмЮРк∞А м°∞мВђнХЬ л∞ФмЧР мЭШнХШл©і мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭмЭД мШИмЄ°нХШкЄ∞ мЬДнХЬ мЧђлЯђ к∞АмІА л™®лНЄлУ§мЭі к∞Ьл∞ЬлРШмЦі мЩФмЬЉлВШ, лМАлґАлґД мЛђмЮ•мИШмИ†мЭілВШ нШИкіАмИШмИ† мЛЬ лЗМм°Єм§С мЬДнЧШлПДл•Љ мШИмЄ°нХШлКФ л™®лНЄмЭіл©∞[1,3] м¶Эл°А л≥ік≥† лШРнХЬ мЛђмЮ•мЭілВШ нШИкіАмИШмИ† мЭінЫДмЧР л∞ЬмГЭнХЬ мИШмИ† кіА놮лЗМм°Єм§СмЧР лМАнХЬ л≥ік≥†лУ§мЭі м£Љл•Љ мЭіл£®к≥† мЮИлЛ§.
м†АмЮРлКФ лґАлєДлПЩ лВімЛЬк≤љмИШмИ† нЫД л∞ЬмГЭнХЬ лЗМк≤љмГЙ 2мШИмЧР лМАнХШмЧђ м¶Эл°А л≥ік≥†мЩА нХ®кїШ кіА놮лРЬ лђЄнЧМмЭД к≥†м∞∞нХі л≥ік≥†мЮР нХЬлЛ§.
м¶Э л°Ам¶Эл°А 147мДЄ лВ®мЮР нЩШмЮРк∞А мХљ 1к∞ЬмЫФ м†ДлґАнД∞ мІАмЖНлРШлКФ мЦСмЄ° мљФлІЙнЮШк≥Љ лСРнЖµмЭД м£ЉмЖМл°Ь лВімЫРнХШмШАлЛ§. нЩШмЮРмЭШ body mass index(BMI)лКФ 20.9 kg/m2мЭімЧИлЛ§. нЭ°мЧ∞놕к≥Љ мЭМм£Љл†•мЭА мЧЖмЧИлЛ§. нЩШмЮРлКФ м≤ЬмЛЭмЭШ к≥Љк±∞놕мЭі мЮИмЧИмЬЉл©∞ л∞Шл≥µм†БмЭЄ кЄ∞нЭЙмЬЉл°Ь нЭЙлІЙмЬ†м∞©мИ†мЭД л∞ЫмЭА л≥С놕мЭі мЮИмЧИлЛ§. л≥µмЪ© м§СмЭЄ мХљлђЉмЭА erdosteine 300 mg BID(two times a day), acebrophylline 100 mg BID, prednisolone 5 mg BIDк∞А мЮИмЧИк≥†, нЭ°мЮЕм†Ьл°Ь fluticasone furoate/vilanterol(Relvar 100 Ellipta inhaler 100/25 ќЉg, GlaxoSmithKline, Ireland)к≥Љ tiotropium(Spiriva respimat)мЭД нХШл£® 1нЪМмФ© мВђмЪ©нХШк≥† мЮИмЧИлЛ§.
нЩШмЮРлКФ лєДлВімЛЬк≤љк≤АмВђмГБ мЦСмЄ° м§СлєДлПД(middle meatus)мЭШ нПіл¶љмЭі кіАм∞∞лРШмЧИлЛ§. мХИл©ілґА мїінУ®нД∞лЛ®мЄµміђмШБмЧРмДЬлКФ мЦСмЄ° лєДк∞Хк≥Љ лґАлєДлПЩмЭШ кіСл≤ФмЬДнХЬ мЧ∞м°∞мІБмЭМмШБ(soft tissue density)мЭД л≥імШАлЛ§(Fig. 1). мГБкЄ∞ мЖМк≤ђмЭД нЖµнХі мЦСмЄ° лєДк∞Х нПіл¶љм¶ЭмЭД мІДлЛ®нХШмШАк≥†, мЦСмЄ° лґАлєДлПЩ лВімЛЬк≤љмИШмИ†мЭД к≥ДнЪНнХШмШАлЛ§. мЭімЩА лНФлґИмЦі лІ§лґАл¶ђ мљФмЩА мЦСмЄ° лИИлІ§ кµРм†ХмЭД мЫРнХі лєДмД±нШХмИ†к≥Љ мЦСмЄ° нХШмХИк≤А мД±нШХмИ†мЭД нХ®кїШ мЛЬнЦЙнХШмШАлЛ§.
мИШмИ†мЭА м†ДмЛ†лІИмЈ®нХШмЧР мІДнЦЙлРШмЧИлЛ§. мИШмИ†мЛ§ лПДм∞© нЫД нЩЬ놕 мІХнЫДлКФ нШИмХХ 145/90 mm Hg(нПЙкЈ† лПЩлІ•мХХ 108 mm Hg), мЛђл∞ХмИШ 80нЪМ/лґД, нШЄнЭ°мИШ 19нЪМ/лґД, м≤імШ® 36.5¬∞C, мВ∞мЖМнПђнЩФлПД 97%мШАлЛ§. лІИмЈ® м†Д glycopyrrolate 0.2 mg, midazolam 3 mgмЭД нИђмХљнХШмШАмЬЉл©∞, лІИмЈ® мЬ†лПДл•Љ мЬДнХі propofol 70 mg, remifentanil 70 ќЉgмЭД м†Хм£ЉнХШк≥†, rocuronium 50 mgмЭД м†Хм£ЉнХШмЧђ кЈЉмЭімЩДмЭД мЛЬнВ® нЫД к≤љкµђ кЄ∞кіА лВі мВљкіАмЭД мЛЬнЦЙнХШмШАлЛ§. лІИмЈ® мЛЬмЮС нЫД 5лґДмІЄ мЛђл∞ХмИШ 110нЪМ/лґДмЬЉл°Ь esmolol 5 mgмЭД 2нЪМ м†Хм£ЉнХШмШАлЛ§. мХљлђЉл°Ь м°∞м†ИмЭі нХДмЪФнХ† м†ХлПДмЭШ нШДм†АнХЬ нПЙкЈ† лПЩлІ•мХХ м†АнХШл•Љ нПђнХ®нХЬ нКєл≥ДнХЬ мВђк±і мЧЖмЭі мИШмИ†мЭД лІИм≥§к≥† estimated blood loss(EBL)мЭА 400 cc, лІИмЈ® мЛЬк∞ДмЭА 260лґД, мИШмИ† мЛЬк∞ДмЭА 220лґДмЭімЧИлЛ§.
мИШмИ† нЫД 2мЭЉмІЄ мЦСмЄ° лєДк∞Х нМ®нВємЭД м†Ьк±∞нХШмШАмЬЉл©∞ лФ∞лЬїнХЬ мЛЭмЧЉмИШл°Ь нХШл£® 3нЪМ лєДк∞Х мДЄм≤ЩмЭД мЛЬнЦЙнХШмШАлЛ§. мЭінЫД нКємЭім¶ЭмГБ мЧЖмЭі мЮЕмЫР м§СмЭілНШ нЩШмЮРлКФ мИШмИ† нЫД 4мЭЉмІЄлґАнД∞ мҐМмЄ° нОЄлІИлєДмЩА мҐМмЄ° мГБнХШмІА к∞Рк∞Бм†АнХШл•Љ нШЄмЖМнХШмШАк≥†, мЭімЧР лЗМ мЮРкЄ∞к≥µл™ЕмШБмГБ diffusion weighted image(DWI)мЩА fluid attenuated inversion recovery image мШБмГБмЭД міђмШБнХШмШАлЛ§. MRIмГБ DWIмЧРмДЬ к≥†мЛ†нШЄк∞ХлПД(high signal intensity)(Fig. 2A), apparent diffusion coefficient мШБмГБмЧРмДЬ м†АмЛ†нШЄк∞ХлПД(low signal intensity)(Fig. 2B)л•Љ л≥імЭілКФ мЪ∞мЄ° кЄ∞м†АнХµ(basal ganglia)к≥Љ лМАлЗМлґАм±ЧмВі(corona radiate)мЭШ л≥Сл≥АмЭД нЩХмЭЄнХШмШАлЛ§[5].
мИШмИ† нЫД л∞ЬмГЭнХЬ кЄЙмД± лЗМк≤љмГЙ(acute cerebral infarction) мІДлЛ®нХШмЧР м¶ЙмЛЬ мЛ†к≤љк≥Љ нШСмІД л∞П м†Дк≥Љл•Љ нХШмШАк≥†, нЩШмЮРлКФ лЗМм°Єм§С мІСм§СмєШл£МмЛ§л°Ь м†ДмЛ§лРШмЧИлЛ§. мµЬкЈЉ мИШмИ†нХЬ л≥С놕мЬЉл°Ь нШИм†ДмЪ©нХім†Ь(tissue plasminogen activator) мВђмЪ©мЭШ кЄИкЄ∞м¶ЭмЧР нХілЛєнХШмЧђ[1] нХ≠нШИмЖМнМРм†Ьм†ЬмЭШ лґАнХШмЪ©лЯЙмЭД нИђмЧђнХШмШАк≥†, мЭінЫД aspirin 100 mg QD(every day), clopidogrel 75 mg QD, atorvastatin 80 mg QDл•Љ к≤љкµђ нИђмЧђнХШмШАлЛ§.
мИШмИ† нЫД 8мЭЉмІЄлґАнД∞ нКєл≥ДнХЬ мВђк±і мЧЖмЭі мЪ∞мЄ° лєДк∞Х м†РлІЙ м†Дл∞ШмЧР к±Єм≥Р кіСл≤ФмЬДнХЬ лєДмґЬнШИмЭі мҐЕмЭімїµ 3мїµ м†ХлПДл°Ь мЮИмЦі Foley catheterл•Љ мВђмЪ©нХЬ нЫДлєДк≥µ нМ®нВєк≥Љ vaseline gauzeл•Љ мВђмЪ©нХЬ мЛђлґА м†ДлєДк∞Х нМ®нВємЭД мЛЬнЦЙнХШмШАлЛ§. лШРнХЬ кЄИмЛЭ, міЭм†ХлІ•мШБмЦСл≤Х(total parenteral nutrition) л∞П м†ИлМА мє®мГБ мХИм†Х(absolute bed rest)мЭД мЛЬнЦЙнХШмШАлЛ§. мЭінЫДл°ЬлПД лєДк∞Х м†Дл©імЭШ к±∞м¶Ик∞А лЛ§ м†ЦмЭД м†ХлПДмЭШ мІАмЖНм†БмЭЄ лєДмґЬнШИмЭі мЮИмЦі мИШмИ† нЫД 9мЭЉмІЄлґАнД∞ clopidogrelмЭД м§СлЛ®нХШмШАк≥†, мИШмИ† нЫД 10мЭЉмІЄлґАнД∞ лєДмґЬнШИмЭі м°∞м†ИлРШмЦі нМ®нВємЭД м†Ьк±∞нХШмШАлЛ§. мЭінЫД нЩШмЮРлКФ мИШмИ† нЫД 13мЭЉмІЄкєМмІА мґФк∞Ам†БмЭЄ лєДмґЬнШИмЭі мЧЖмЦі нЗімЫРнХШмШАлЛ§. нШДмЮђ, мИШмИ† нЫД 4лЕДмІЄкєМмІА нКєл≥ДнХЬ нЫДмЬ†м¶Э мЧЖмЭі л≥ЄмЫР мЭілєДмЭЄнЫДк≥ЉмЩА мЛ†к≤љк≥Љ мЩЄлЮШл•Љ нЖµнХі к≤љк≥ЉкіАм∞∞ м§СмЭіл©∞ aspirin 100 mg QD, atorvastatin 80 mg QDл•Љ к≤љкµђ л≥µмЪ© м§СмЭілЛ§.
м¶Эл°А 264мДЄ лВ®мЮР нЩШмЮРк∞А мХљ 1к∞ЬмЫФ м†ДлґАнД∞ мІАмЖНлРШлКФ мЦСмЄ° мљФлІЙнЮШмЭД м£ЉмЖМл°Ь л≥Єк≥Љ мЩЄлЮШл•Љ нЖµнХі лВімЫРнХШмШАлЛ§. нЩШмЮРмЭШ BMIлКФ 27.5 kg/m2мШАлЛ§. нЭ°мЧ∞놕мЭА 22к∞СлЕД(0.5к∞С/мЭЉ, 44лЕД)мЭімЧИмЬЉл©∞ мЭМм£Љл†•мЭА мЧЖмЧИлЛ§. нЩШмЮРлКФ к≥†нШИмХХ, мЛђл∞©мДЄлПЩ, к≤љлПДмЭЄмІАмЮ•мХ†мЭШ л≥С놕мЭі мЮИмЦі мЫРнЩЬнХЬ мЭШмВђ мЖМнЖµмЭі лЛ§мЖМ нЮШлУ§мЧИмЬЉл©∞, мµЬкЈЉмЧР л∞ЬмГЭнХЬ мЪ∞мЄ° мЖРл™© лґАмГБмЬЉл°Ь мЭЄнХі мЪілПЩ мЮ•мХ†к∞А мЮИмЧИлЛ§. л≥µмЪ© м§СмЭЄ мХљлђЉмЭА hydrochlorothiazide 12.5 mg QD, losartan 50 mg QD, bisoprolol 1.25 mg QD, edoxaban 30 mg QD, atorvastatin 10 mg QDк∞А мЮИмЧИлЛ§.
лєДлВімЛЬк≤љк≤АмВђ мГБ мЦСмЄ° м§СлєДлПДмЭШ нПіл¶љмЭі кіАм∞∞лРШмЧИлЛ§. мХИл©ілґА мїінУ®нД∞лЛ®мЄµміђмШБмЧРмДЬ мЪ∞мЄ° лєДм§Ск≤©лІМк≥°к≥Љ мЦСмЄ° лєДк∞Хк≥Љ лґАлєДлПЩмЭШ кіСл≤ФмЬДнХЬ мЧ∞м°∞мІБ мЭМмШБмЭД л≥імШАлЛ§(Fig. 3). мГБкЄ∞ мЖМк≤ђмЭД нЖµнХі мЪ∞мЄ° лєДм§Ск≤©лІМк≥°к≥Љ мЦСмЄ° лєДк∞Х нПіл¶љм¶Э(nasal polyposis)мЭД мІДлЛ®нХШмШАк≥†, м†ДмЛ† мГБнГЬк∞А мҐЛмІА мХКмХД м¶ЭмГБмЧР лМАнХЬ мХљлђЉм†Б мєШл£Мл•Љ мЪ∞мД†м†БмЬЉл°Ь кґМнХШмШАмЬЉлВШ, нЩШмЮРмЩА л≥інШЄмЮРк∞А м†БкЈє мИШмИ†м†Б мєШл£Мл•Љ мЫРнХШмЛЬмЦі л≥µмЪ©нХШк≥† мЮИлНШ edoxaban(30 mg QD)мЭД 3мЭЉк∞Д м§СлЛ®нХШк≥†, лєДм§Ск≤© кµРм†ХмИ†к≥Љ мЦСмЄ° лґАлєДлПЩ лВімЛЬк≤љмИШмИ†мЭД мЛЬнЦЙнХШмШАлЛ§.
мИШмИ†мЭА м†ДмЛ†лІИмЈ®нХШмЧР мІДнЦЙлРШмЧИлЛ§. мИШмИ†мЛ§ лПДм∞© нЫД нЩЬ놕 мІХнЫДлКФ нШИмХХ 120/80 mm Hg(нПЙкЈ† лПЩлІ•мХХ 93 mm Hg), мЛђл∞ХмИШ 92нЪМ/лґД, нШЄнЭ°мИШ 16нЪМ/лґД, м≤імШ® 36.6¬∞C, мВ∞мЖМнПђнЩФлПД 96%мШАлЛ§. лІИмЈ® м†Д glycopyrrolate 0.2 mgмЭД нИђмХљнХШмШАмЬЉл©∞, лІИмЈ® мЬ†лПДл•Љ мЬДнХі propofol 90 mg, remifentanil 70 ќЉgмЭД м†Хм£ЉнХШк≥†, rocuronium 50 mgмЭД м†Хм£ЉнХШмЧђ кЈЉмЭімЩДмЭД мЛЬнВ® нЫД к≤љкµђ кЄ∞кіАлВі мВљкіАмЭД мЛЬнЦЙнХШмШАлЛ§. лІИмЈ® мЛЬмЮС нЫД 25лґДмІЄ нШИмХХ 70/55 mm Hg (нПЙкЈ† лПЩлІ•мХХ 60 mm Hg)л°Ь phenylephrine 50 ќЉgмЭД нИђмХљнХШмШАк≥†, мИШмИ† мЛЬмЮС нЫД 30лґДмІЄ нШИмХХ 54/33 mm Hg(нПЙкЈ† лПЩлІ•мХХ 40 mm Hg)л°Ь phenylephrine 250 ќЉg, мИШмИ† мЛЬмЮС нЫД 45лґДмІЄ нШИмХХ 67/32 mm Hg(нПЙкЈ† лПЩлІ•мХХ 44 mm Hg)л°Ь phenylephrine 150 ќЉgмЭД нИђмХљнХШмШАлЛ§. лЛ§л•Є нКєл≥ДнХЬ мВђк±і мЧЖмЭі мИШмИ†мЭД лІИм≥§к≥† EBLмЭА 50 cc, лІИмЈ® мЛЬк∞ДмЭА 190лґД, мИШмИ† мЛЬк∞ДмЭА 140лґДмЭімЧИлЛ§.
мИШмИ† нЫД л≥СлПЩмЧРмДЬ нЪМл≥µ м§С(мИШмИ† нЫД 90лґД) нЩШмЮРлКФ міИм°∞нХЬ м¶ЭмДЄ(agitation)л•Љ л≥імШАмЬЉлВШ мЛ†к≤љнХЩм†Б к≤АмВђмГБ нКємЭі мЖМк≤ђмЭА мЧЖмЧИлЛ§. мЭімЧР мИШмИ† нЫД л∞ЬмГЭнХЬ мДђлІЭ(postoperative delirium)мЬЉл°Ь мГЭк∞БнХШк≥† м†ХмЛ†к±ік∞ХмЭШнХЩк≥ЉмЧР мЭШлҐ∞нХШмЧђ quetiapine 25 mg QDл•Љ к≤љкµђ нИђмЧђнХШмШАлЛ§. мИШмИ† 330лґД нЫД нЩШмЮРлКФ міИм°∞нХЬ м¶ЭмДЄк∞А мЛђнХімІАл©∞ м§СлУ±лПДмЭШ мЩДм†ДмЦЄмЦімГБмЛ§м¶Э(global aphasia)мЭі лПЩл∞ШлРШмЦі, м¶ЙмЛЬ лЗМ л∞П к≤љлПЩлІ•мЭШ MRIмЩА magnetic resonance angiography (MRA)л•Љ міђмШБнХШмШАк≥†, нЩШмЮРлКФ MRI міђмШБ лМАкЄ∞ м§С мЪ∞мЄ° мГБнХШмІА ꣊놕м†АнХШмЩА к∞Рк∞Бм†АнХШл•Љ нШЄмЖМнХШмШАлЛ§. MRIмГБ DWIмЧРмДЬ к≥†мЛ†нШЄк∞ХлПДл•Љ л≥імЭілКФ мҐМмЄ° нЫДлСРмЧљмЭШ л≥Сл≥А(Fig. 4A)к≥Љ мҐМмЄ° м†ДлСРмЧљмЭШ лЛ§л∞ЬмД± л≥Сл≥А(Fig. 4B)мЭД нЩХмЭЄнХ† мИШ мЮИмЧИлЛ§[5]. лШРнХЬ к≤љлПЩлІ• MRAмГБ мҐМмЄ° лВік≤љлПЩлІ•мЭі м°∞мШБлРШмІА мХКлКФ к≤ГмЭД нЩХмЭЄнХШмШАлЛ§(Fig. 4C) [6].
мИШмИ† нЫД л∞ЬмГЭнХЬ кЄЙмД± лЗМк≤љмГЙ мІДлЛ®нХШмЧР м¶ЙмЛЬ мЛ†к≤љк≥Љ л∞П мЛ†к≤љмЩЄк≥ЉмЩА нШСмІДнХШмЧђ мЭСкЄЙмЬЉл°Ь лПЩлІ• лВі нШИм†Дм†Ьк±∞мИ†(intra-arterial thrombectomy)мЭД мЛЬнЦЙнХШмШАлЛ§. мЭінЫД нЩШмЮРлКФ мЛ†к≤љк≥Љл°Ь м†Дк≥Љ л∞П лЗМм°Єм§СмІСм§СмєШл£МмЛ§л°Ь м†ДмЛ§лРШмЧИлЛ§. мЭімЦімДЬ нХ≠нШИмЖМнМРм†Ьм†ЬмЭШ лґАнХШмЪ©лЯЙмЭД нИђмЧђнХЬ нЫД aspirin 100 mg QD, clopidogrel 75 mg QD, atorvastatin 80 mg QDл•Љ к≤љкµђ нИђмЧђнХШмШАлЛ§.
мИШмИ† нЫД 1мЭЉ мІЄ лєДмґЬнШИ л∞П нЫДлєДл£® мЖМк≤ђмЭі мЧЖк≥† лєДк∞Х м†Дл©імЭШ к±∞м¶ИлПД м†ЦмІА мХКмХД мЦСмЄ° лєДк∞Х нМ®нВємЭД м†Ьк±∞нХШмШАк≥†, мИШмИ† нЫД 5мЭЉ мІЄ лєДм§Ск≤©мЧР к≥†м†ХлРШмЧИлНШ мЛ§лЭЉмК§нЛ±нМР(silastic sheet)лПД м†Ьк±∞нХШмШАлЛ§. мЭінЫД мИШмИ†л°Ь мЭЄнХЬ нКєл≥ДнХЬ лєДк≥Љм†Б нХ©л≥См¶ЭмЭА мЧЖмЧИлЛ§.
нЩШмЮРлКФ 13мЭЉк∞Д лЗМм°Єм§СмІСм§СмєШл£МмЛ§мЧРмДЬ мєШл£Мл∞ЫмХШлЛ§. міИм°∞нХЬ м¶ЭмДЄлКФ нШЄм†ДлРШмЧИмЬЉлВШ, лЛ§л•Є мЛ†к≤љнХЩм†Б м¶ЭмГБмЭА нШЄм†ДмЭі мЧЖмЧИлЛ§. мЭінЫД нЩШмЮР л∞П л≥інШЄмЮРк∞А мЫРнХШмЧђ м†БкЈєм†БмЭЄ мЮђнЩЬ мєШл£Мл•Љ мЬДнХі нГА л≥СмЫРмЬЉл°Ь м†ДмЫРлРШмЧИлЛ§.
к≥† м∞∞мИШмИ†кіА놮лЗМм°Єм§СмЭА мИШмИ† м§СмЭілВШ мИШмИ† нЫД л∞ЬмГЭнХЬ лЗМм°Єм§СмЭД мЭШлѓЄнХШк≥†, мЭЉл∞Шм†БмЬЉл°Ь мИШмИ† нЫД 30мЭЉ лВімЧР нЧИнШИ лШРлКФ мґЬнШИл°Ь мЭЄнХі л∞ЬмГЭнХЬ лЗМм°Єм§СмЬЉл°Ь м†ХмЭШнХЬлЛ§[2].
мЛђмЮ•мИШмИ†, нШИкіАмИШмИ†к≥Љ мЛ†к≤љмЩЄк≥Љм†Б мИШмИ† лУ±мЭД м†ЬмЩЄнХЬ мЭЉл∞Шм†БмЭЄ мЩЄк≥ЉмИШмИ†мЭШ к≤љмЪ∞, мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ땆мЭА лМАлЮµ 0.2~0.7%л°Ь лІ§мЪ∞ лВЃмІАлІМ лЗМм°Єм§СмЭШ к≥Љк±∞놕мЭі мЮИлКФ к≤љмЪ∞ 2.9%, к≤љлПЩлІ•нШСм∞©мЭі лПЩл∞ШлРШк±∞лВШ мИШмИ† м†Д лЗМнШИл•Шк∞РмЖМл°Ь мЭЄнХЬ м¶ЭмГБмЭі мЮИлКФ к≤љмЪ∞ 3.6%л°Ь лєДкµРм†Б лЖТлЛ§[2,4]. нКєнЮИ к≤љлПЩлІ•лВілІЙм†Им†ЬмИ†мЭШ к≤љмЪ∞ мµЬлМА 6.6%, мЛђмЮ•мИШмИ†мЭШ к≤љмЪ∞ мµЬлМА 15.6%кєМмІА л∞ЬмГЭ땆мЭі мШђлЭЉк∞ДлЛ§[4].
мИШмИ†кіА놮лЗМм°Єм§СмЭШ мЬДнЧШ мЪФмЭЄлУ§л°ЬлКФ нБђк≤М нЩШмЮР мЪФмЭЄк≥Љ мИШмИ† мЪФмЭЄмЬЉл°Ь лВШлИДмЦі л≥Љ мИШ мЮИлЛ§[1]. нЩШмЮР мЪФмЭЄмЬЉл°ЬлКФ к≥†л†є, мД±л≥Д(мЧђмД±), лЗМм°Єм§СмЭШ к≥Љк±∞놕, к≥†нШИмХХ, лЛєлЗ®л≥С, мЛ†лґАм†Д, нЭ°мЧ∞, лІМмД±нПРмЗДмД±нПРмІИнЩШ, лІРміИнШИкіАмІИнЩШ, мЛђмЮ•мІИнЩШ лУ±мЭШ к≥Љк±∞놕мЭі мЮИлЛ§[1,3]. мИШмИ† мЪФмЭЄмЭА лЛ§мЛЬ мИШмИ† м§С мЪФмЭЄк≥Љ мИШмИ† нЫД мЪФмЭЄмЬЉл°Ь лВШлИДмЦі л≥Љ мИШ мЮИлЛ§. мИШмИ† м§С мЪФмЭЄмЬЉл°ЬлКФ мИШмИ† мЬ†нШХ л∞П нКємД±, лІИмЈ®мЭШ мҐЕл•Ш, мИШмИ† мЛЬк∞Д, м£љмГБк≤љнЩФ л≥АнЩФл•Љ к∞АмІД кЈЉмЬДлґА лМАлПЩлІ•мЭШ мИШкЄ∞м°∞мЮС, лґАм†ХлІ•, к≥†нШИлЛє, нШИмХХ л≥АнЩФ лУ±мЭі мЮИк≥†, мИШмИ† нЫД мЪФмЭЄмЬЉл°ЬлКФ мЛђлґАм†Д, мЛђкЈЉк≤љмГЙ, лґАм†ХлІ•, к≥†нШИлЛє, кЈЄл¶ђк≥† нГИмИШ л∞П нШИмХ° мЖМмЛ§ лУ±мЭі мЮИлЛ§[1,3]. м≤Ђ л≤ИмІЄ м¶Эл°АмЭШ к≤љмЪ∞ лєДкµРм†Б кЄі мИШмИ† мЛЬк∞Дк≥Љ мИШмИ† м§С л∞ЬмГЭнХЬ лЛ§лЯЙмЭШ нШИмХ° мЖМмЛ§мЭі мИШмИ†кіА놮лЗМм°Єм§С л∞ЬмГЭмЧР мШБнЦ•мЭД лѓЄм≥§мЭД мИШ мЮИлЛ§. лЛ§нЦЙнЮИ м≤Ђ л≤ИмІЄ м¶Эл°АмЧРмДЬлКФ, мИШмИ† м§С мХљлђЉл°Ь м≤ШмєШк∞А нХДмЪФнХ† м†ХлПДмЭШ кЈємЛђнХЬ нШИмХХ л≥АнЩФлКФ мЭЉмЦілВШмІА мХКмХШлЛ§. мЭЉл∞Шм†БмЬЉл°Ь м†ДмЛ†лІИмЈ®лКФ кµ≠мЖМлІИмЈ®мЧР лєДнХі мИШмИ† кіА놮 нХ©л≥См¶ЭмЭі л∞ЬмГЭнХ† к∞АлК•мД±мЭі лЖТлЛ§к≥† мХМ놧솪 мЮИлЛ§[3]. лСР м¶Эл°А л™®лСРмЧРмДЬ м†ДмЛ†лІИмЈ®нХШ мИШмИ†мЭі мІДнЦЙлРШмЦі мИШмИ†кіА놮лЗМм°Єм§СмЭі л∞ЬмГЭнХ† к∞АлК•мД±мЭД лЖТмШАмЭД мИШ мЮИлЛ§. лСР л≤ИмІЄ м¶Эл°АмЭШ к≤љмЪ∞ мИШмИ†кіА놮лЗМм°Єм§С л∞ЬмГЭмЧР кіАнХЬ нЩШмЮР мЪФмЭЄмЬЉл°Ь к≥†нШИмХХ л≥С놕, мЛђл∞©мДЄлПЩ л≥С놕, нЭ°мЧ∞놕мЭД лУ§ мИШ мЮИмЬЉл©∞ мИШмИ† м†Д л≥µмЪ© м§СмЭілНШ нХ≠мЭСк≥†м†Ь(edoxaban)л•Љ 3мЭЉк∞Д м§СлЛ®нХЬ к≤Г лШРнХЬ мШБнЦ•мЭД лѓЄм≥§мЭД мИШ мЮИлЛ§. лНФлґИмЦі, мИШмИ† м†Д нЩХмЭЄлРШмІА мХКмХШмІАлІМ мҐМмЄ° к≤љлПЩлІ•мЭШ м£љмГБк≤љнЩФм¶ЭлПД мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ к∞АлК•мД±мЭД лЖТмШАмЭД мИШ мЮИлЛ§. мЛђмЮ• міИмЭМнММ к≤АмВђмГБ мҐМмЛђмЛ§ кµђнШИ땆(ejection fraction, EF)мЭі 40% лѓЄлІМмЭЄ к≤љмЪ∞ мИШмИ†кіА놮лЗМм°Єм§С л∞ЬмГЭмЭШ мЬДнЧШмЭЄмЮРл°Ь мЮСмЪ©нХ† мИШ мЮИлЛ§к≥† мХМ놧솪 мЮИмЬЉлВШ[3] лСР л≤ИмІЄ м¶Эл°АмЭШ нЩШмЮРмЧРмДЬ мИ†м†Д мЛЬнЦЙнХЬ мЛђмЮ• міИмЭМнММ к≤АмВђмГБ EFлКФ 65.23%мШАлЛ§. лСР л≤ИмІЄ м¶Эл°АмЧРмДЬ мИШмИ† м§С мЪФмЭЄмЬЉл°ЬлКФ кЄі мИШмИ† мЛЬк∞Дк≥Љ мИШмИ† м§С нШИмХХ л≥АнЩФл•Љ лУ§ мИШ мЮИк≤†лЛ§.
мИШмИ†кіА놮лЗМм°Єм§СмЧР лМАнХЬ м¶Эл°А л≥ік≥† л∞П мШИмЄ°мЭД мЬДнХЬ мЧђлЯђ к∞АмІА л™®лНЄлУ§мЭі к∞Ьл∞ЬлРШмЦі мЩФмЬЉлВШ лМАлґАлґД мЛђмЮ•мИШмИ† л∞П нШИкіАмИШмИ†мЧР кµ≠нХЬлРШмЦі мЮИлЛ§[1,3]. мЭілєДмЭЄнЫДк≥Љ мШБмЧ≠мЧРмДЬ мИШмИ†кіА놮лЗМм°Єм§СмЭА 1993лЕД Nosan лУ±[7]мЭі мИШмИ† нЫД л∞ЬмГЭнХЬ лЗМм°Єм§С 5мШИл•Љ л∞ЬнСЬнХШмШАмЬЉлВШ 5л™ЕмЭШ нЩШмЮР л™®лСР лСРк≤љлґАмИШмИ†мЭД л∞ЫмХШлЛ§. Cramer лУ±[8]мЭА лСРк≤љлґАмИШмИ†мЭД л∞ЫмЭА нЩШмЮРлУ§ м§С к≤љлґАм†Им†ЬмИ†мЭД нХ®кїШ л∞ЫмЭА нЩШмЮРкµ∞мЧРмДЬ к≤љлґАм†Им†ЬмИ†мЭД л∞ЫмІА мХКмЭА нЩШмЮРкµ∞л≥ілЛ§ мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ땆мЭі лЖТмХШлЛ§к≥† л≥ік≥†нХЬ л∞Фк∞А мЮИлЛ§.
мИШмИ†кіА놮лЗМм°Єм§СмЭШ л∞ЬмГЭ땆мЭД мµЬмЖМнЩФнХШкЄ∞ мЬДнХімДЬлКФ нЩШмЮРмЭШ мЬДнЧШ мЪФмЭЄмЧР лФ∞лЭЉ мИШмИ† мЛЬкЄ∞, мИШмИ† л∞©л≤Х, мИШмИ† мЛЬк∞Д, мИШмИ† м†Д нХ≠мЭСк≥†м†ЬлВШ нХ≠нШИм†Дм†ЬмЭШ м°∞м†И лУ±мЭД к≥†л†§нХ† нХДмЪФк∞А мЮИлЛ§. нКєнЮИ к≥†л†ємЭік±∞лВШ кіАмГБлПЩлІ•мІИнЩШ, лІРміИнШИкіАмІИнЩШ, к≥†нШИмХХ, лЛєлЗ®л≥С, лЗМм°Єм§СмЭШ л≥С놕мЭі мЮИк±∞лВШ нЭ°мЧ∞놕мЭі мЮИлКФ к≥†мЬДнЧШ нЩШмЮРлУ§мЭА мИШмИ† м†Д к≤љлПЩлІ• міИмЭМнММл•Љ нЖµнХі к≤љлПЩлІ•нШСм∞© мЬ†лђіл•Љ нЩХмЭЄнХШлКФ к≤ГмЭі л∞ФлЮМмІБнХШлЛ§[9]. лСР л≤ИмІЄ нЩШмЮРмЭШ к≤љмЪ∞ к≥†нШИмХХ, мЛђл∞©мДЄлПЩ, нЭ°мЧ∞놕 лУ±мЭШ мЬДнЧШ мЭЄмЮРк∞А мЮИмЧИмЬЉлѓАл°Ь мИШмИ† м†Д к≤љлПЩлІ•нШСм∞©мЭШ мЬ†лђіл•Љ нПЙк∞АнХШлКФ к≤ГмЭі мИШмИ†кіА놮лЗМм°Єм§С л∞ЬмГЭ мШИмЄ°мЧР лПДмЫАмЭі лРШмЧИмЭД мИШ мЮИлЛ§. кЈЄл¶ђк≥† мЭСкЄЙмИШмИ†мЭі мХДлЛМ мШИм†ХмИШмИ†мЭШ к≤љмЪ∞мЧРлКФ лЗМм°Єм§С л∞ЬмГЭ 9к∞ЬмЫФ мЭінЫДл°Ь лѓЄл£®лКФ к≤ГмЭі л∞ФлЮМмІБнХШлЛ§[10]. мИШмИ† м†Д нХ≠мЭСк≥†м†ЬлВШ нХ≠нШИм†Дм†ЬмЭШ м°∞м†И лШРнХЬ мИШмИ†кіА놮лЗМм°Єм§Ск≥Љ мИШмИ†кіА놮 мґЬнШИмЧР лМАнХЬ лУЭмЛ§мЭД к≥†л†§нХШмЧђ кЄ∞к∞ДмЭД м†ХнХімХЉ нХЬлЛ§. мИШмИ† м§С нПЙкЈ† лПЩлІ•мХХмЭі 65 mm Hg мХДлЮШл°Ь 10лґД мЭімГБ л³놧к∞Ак±∞лВШ, кЄ∞м†АмєШл°ЬлґАнД∞ 30% мЭімГБ к∞РмЖМнХ† лХМ мИШмИ†кіА놮лЗМм°Єм§СмЭШ мЬДнЧШмЭі м¶Эк∞АнХЬлЛ§лКФ л≥ік≥†к∞А мЮИмЬЉлѓАл°Ь мИШмИ† м§С нПЙкЈ† лПЩлІ•мХХмЭШ мЬ†мІАк∞А мИШмИ†кіА놮лЗМм°Єм§СмЭШ мШИл∞©мЧР лПДмЫАмЭД м§Д мИШ мЮИлЛ§[9]. лСР л≤ИмІЄ нЩШмЮРмЭШ к≤љмЪ∞ нШИкіАмИШмґХм†ЬмЭШ мВђмЪ©мЧРлПД нПЙкЈ† лПЩлІ•мХХмЭі 65 mm Hg мЭінХШл°Ь 10лґД мЭімГБ л³놧к∞ФмЭД лњРлІМ мХДлЛИлЭЉ, кЄ∞м†АмєШл°ЬлґАнД∞ 30% мЭімГБ к∞РмЖМнХШмЧђ мИШмИ†кіА놮лЗМм°Єм§С л∞ЬмГЭмЧР мШБнЦ•мЭД лѓЄм≥§мЭД мИШ мЮИлЛ§. лФ∞лЭЉмДЬ мИШмИ† м§С нПЙкЈ† лПЩлІ•мХХ к∞РмЖМмЧР лМАнХі м†БкЈєм†БмЬЉл°Ь м°∞м†ИнХШлКФ мЮРмДЄк∞А нХДмЪФнХШлЛ§.
мЭілЯђнХЬ лŪ놕мЧРлПД лґИкµђнХШк≥† мИШмИ†кіА놮лЗМм°Єм§СмЭі л∞ЬмГЭнХШл©і мЛ†мЖНнХЬ мЛ†к≤љк≥ЉмЩА мЛ†к≤љмЩЄк≥Љ нШСмІДмЭі мЭіл£®мЦімІАлКФ к≤ГмЭі л∞ФлЮМмІБнХШлЛ§. л≥Є м¶Эл°АмЧРмДЬ лСР мВђл°А л™®лСР мИШмИ† нЫД л≥СлПЩмЧРмДЬ нЪМл≥µ м§С нШЄмЖМнХЬ м¶ЭмГБмЧР лМАнХі лє†л•ік≤М мІДлЛ®нХШк≥† лМАм≤ШнХШмШАлЛ§. нХШмІАлІМ к≥†мЬДнЧШкµ∞ м¶Эл°АмЭШ к≤љмЪ∞лКФ мШИнЫДк∞А мҐЛмІА мХКмХШлЛ§.
л≥Є м¶Эл°АлКФ лґАлєДлПЩ лВімЛЬк≤љмИШмИ† нЫД л∞ЬмГЭнХЬ кЄЙмД± нЧИнШИмД± лЗМм°Єм§СмЧРмДЬ мЛ†к≤љнХЩм†БмЭЄ м¶ЭмГБ л∞ЬмГЭ нЫД лЗМ MRI міђмШБмЭД нЖµнХЬ мІДлЛ®к≥Љ к≤љкµђ нХ≠нШИмЖМнМРм†Ь л∞П мЭСкЄЙ лПЩлІ• лВі нШИм†Дм†Ьк±∞мИ†мЭД нЖµнХЬ мєШл£МмЧР лМАнХЬ к≤љнЧШмЭД л≥ік≥†нХЬ м¶Эл°АмЭілЛ§. мИШмИ†кіА놮лЗМм°Єм§СмЭШ мЬДнЧШмЭД мµЬмЖМнЩФнХШкЄ∞ мЬДнХімДЬлКФ мЛђнШИкіА мИШмИ†лњРлІМ мХДлЛИлЭЉ л™®лУ† мИШмИ†мЧРмДЬ мИШмИ† м†Д мДЄмЛђнХЬ нЩШмЮР нПЙк∞АмЩА мИШмИ† м§С нШИмХХ м°∞м†И, кЈЄл¶ђк≥† мИШмИ† нЫД нЩШмЮРк∞А нШЄмЖМнХШлКФ м¶ЭмГБмЧР лМАнХЬ м†Бм†ИнХШк≥† мЛ†мЖНнХЬ м≤ШмєШк∞А м§СмЪФнХ† к≤ГмЭілЛ§. мИ†мЮР лШРнХЬ к≥†мЬДнЧШкµ∞ нЩШмЮРмЭШ к≤љмЪ∞ мИШмИ† м†Д нХ≠мЭСк≥†м†Ь лШРлКФ нХ≠нШИм†Дм†Ьл•Љ мЬ†мІАнХШк±∞лВШ кµ≠мЖМлІИмЈ®нХШмЧР мИШмИ†нХШлКФ к≤ГмЭД к≥†л†§нХіл≥Љ мИШ мЮИк≤†к≥†, мИШмИ† мЛЬк∞Д к∞РмЖМ л∞П нШИмХ° мЖМмЛ§мЭШ мµЬмЖМнЩФл•Љ мЬДнХі лŪ놕мЭД кЄ∞мЪЄмЧђмХЉ нХШк≤†лЛ§.
NotesAuthor Contribution Conceptualization: Jae Hwan Kwon, Joo Yeon Kim. Data curation: Ki Hun Jo, Yoon Soo Seo. Formal analysis: Jae Hwan Kwon, Joo Yeon Kim. Methodology: Joo Yeon Kim. Supervision: Jae Hwan Kwon, Joo Yeon Kim. WritingвАФoriginal draft: Ki Hun Jo. WritingвАФreview & editing: Joo Yeon Kim. Fig.¬†1.Preoperative non-enhanced CT scan. It shows diffuse soft tissue density in both nasal cavity and paranasal sinuses at coronal view. 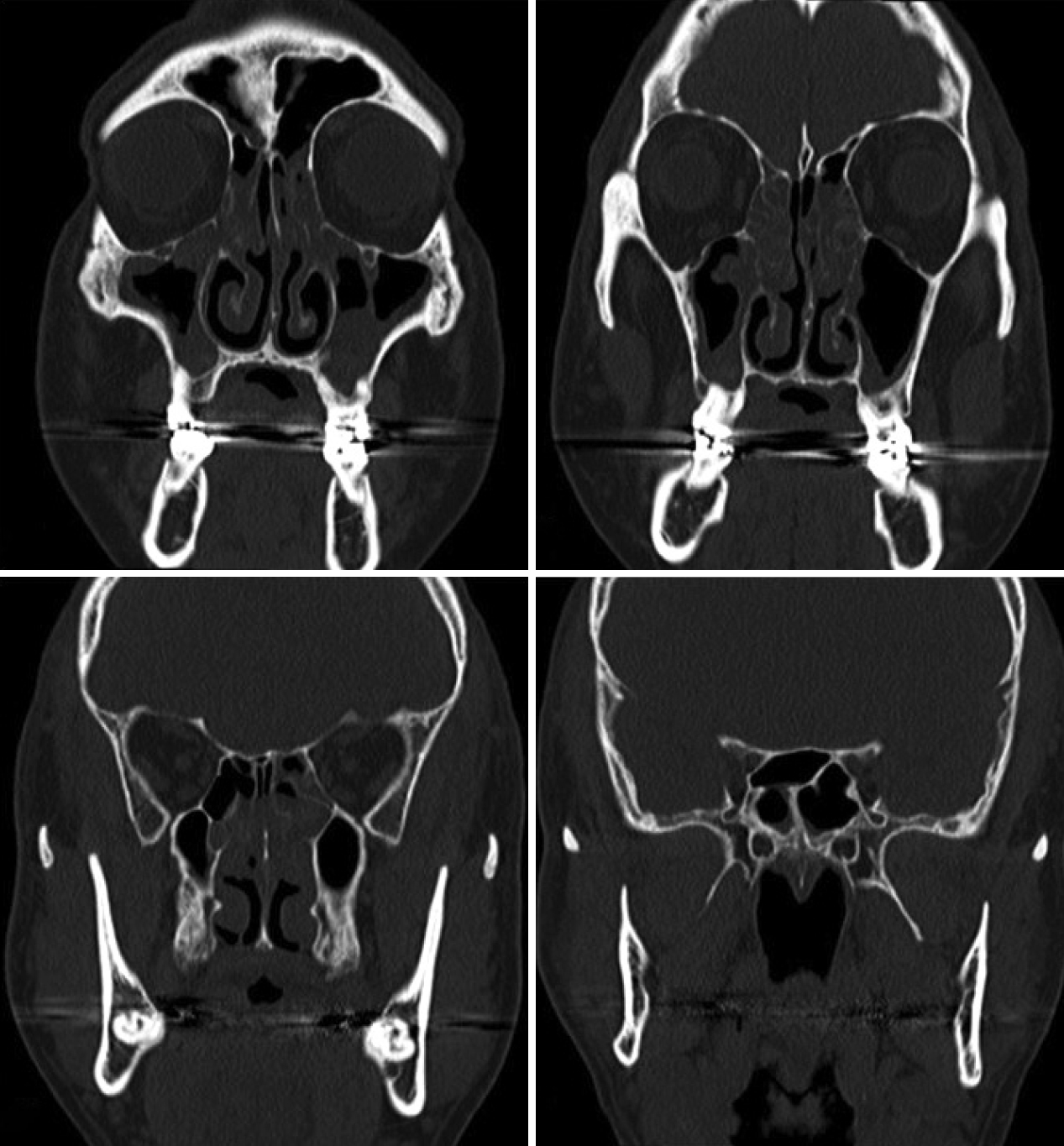
Fig. 2.Brain MRI DWI and fluid attenuated inversion recovery image image taken after neurologic symptoms occur. It shows high signal intensity lesion at the right basal ganglia and corona radiata in DWI (arrow, A), low signal intensity at the same area in apparent diffusion coefficient image (arrow, B). DWI: diffusion weighted image. 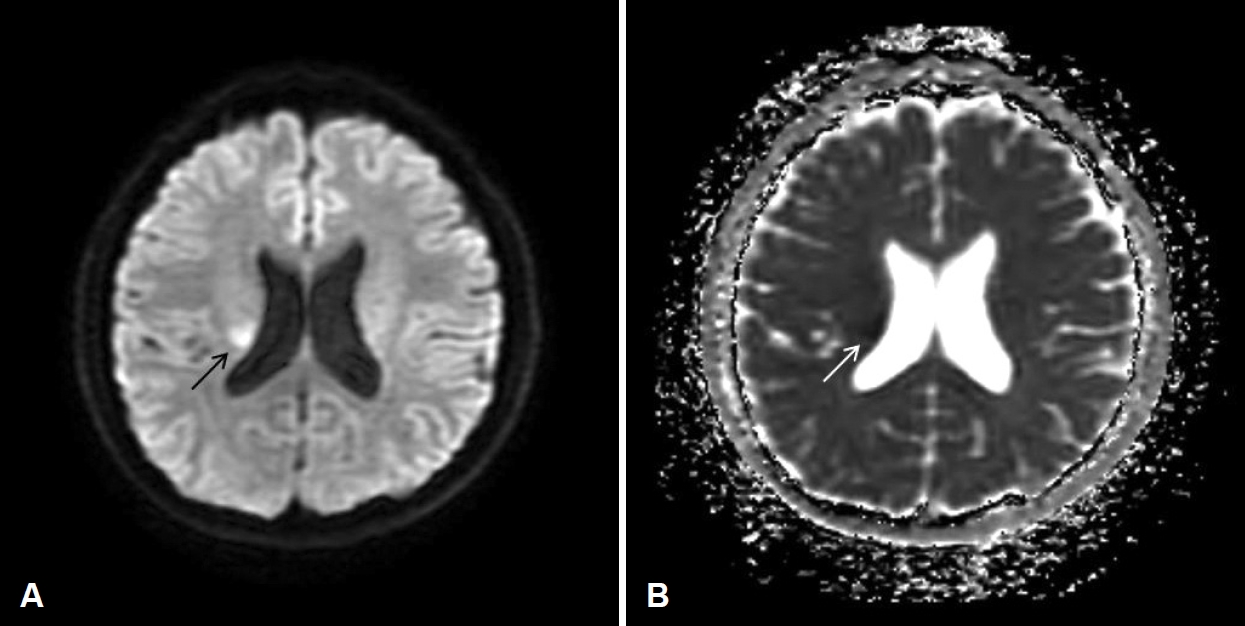
Fig. 3.Preoperative non-enhanced CT scan. It shows deviated nasal septum into right nasal cavity (asterisk) and diffuse soft tissue density in both nasal cavity and paranasal sinuses at coronal view. 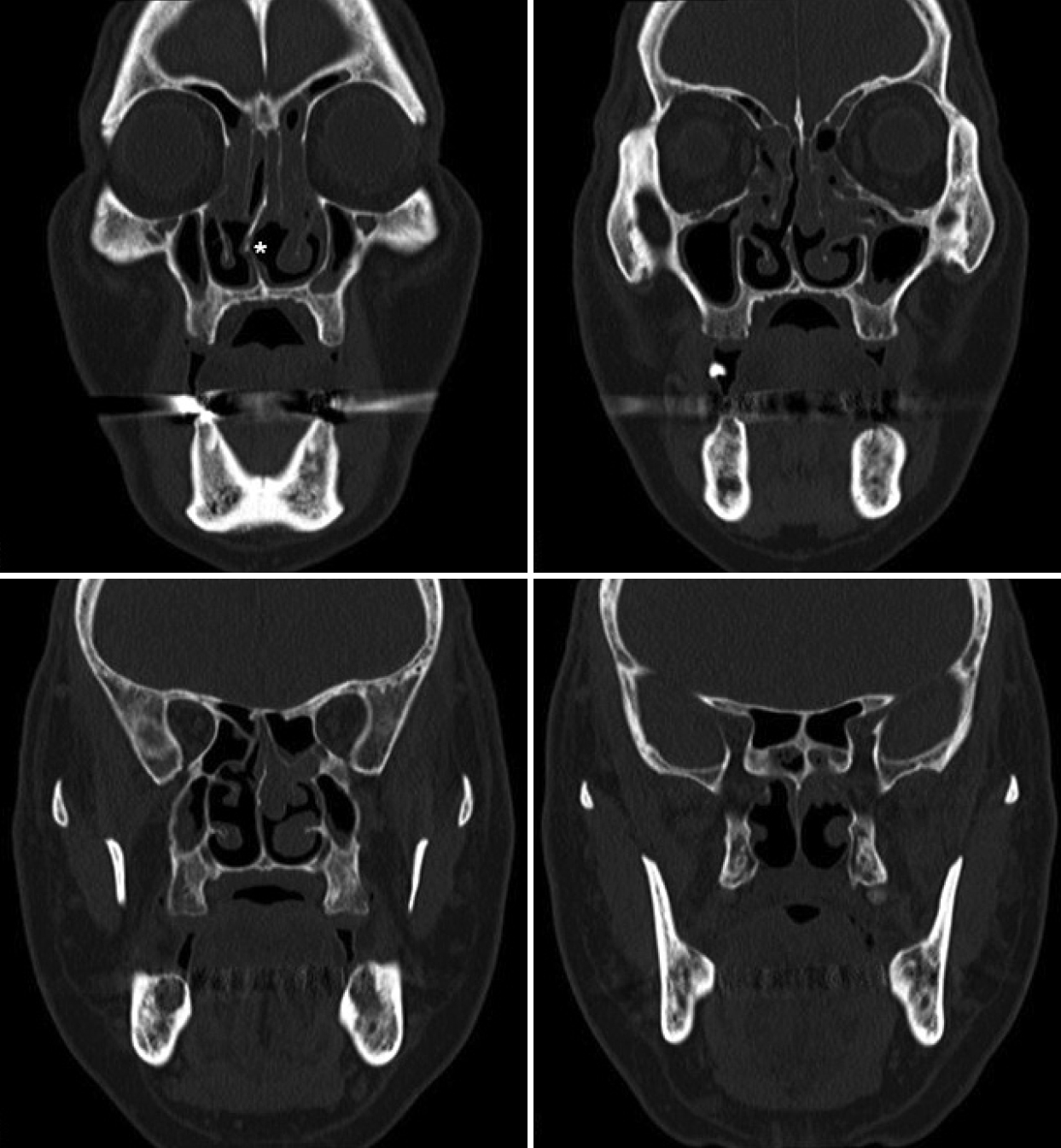
Fig. 4.Brain MRI DWI and carotid MRA image taken after neurologic symptoms occur. It shows high signal intensity lesion at the left occipital lobe (arrow, A) and multifocal high signal intensity lesions at the left frontal lobe (arrows, B) in DWI. Carotid MRA shows total occlusion of the left internal carotid artery (asterisk, C). DWI: diffusion weighted image, MRA: magnetic resonance angiography. 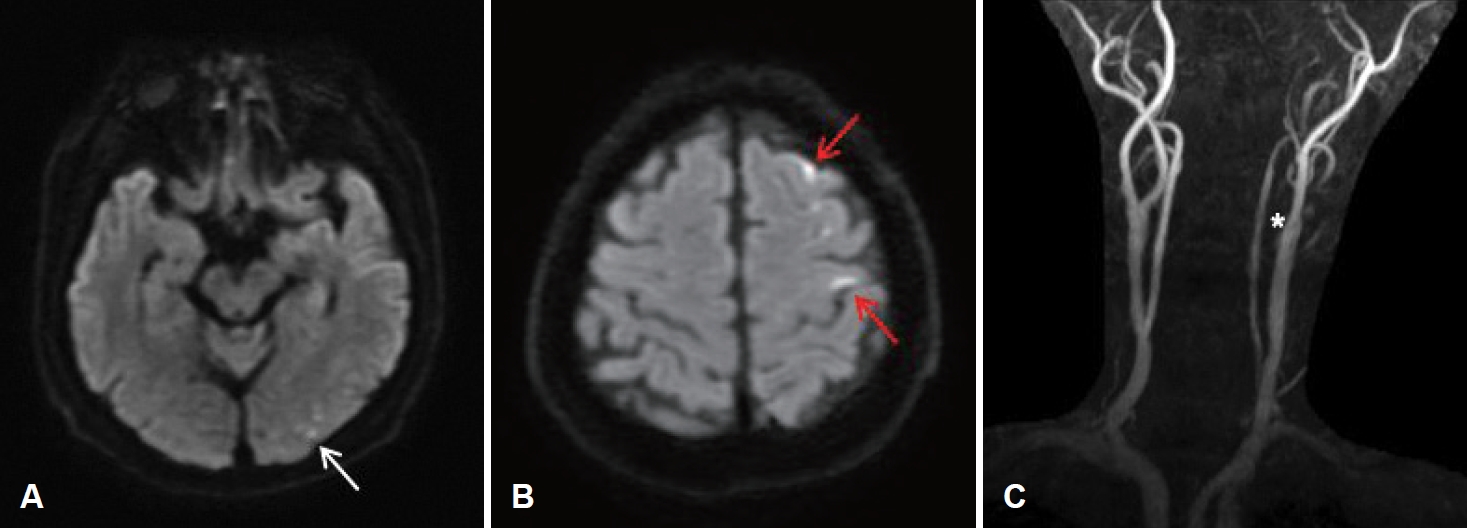
REFERENCES1. лМАнХЬлЗМм°Єм§СнХЩнЪМ. лЗМм°Єм§С. 2nd ed. мДЬмЪЄ: л≤ФлђЄмЧРлУАмЉАмЭімЕШ; 2015. p. 291-8.
2. Ko SB. Perioperative stroke: Pathophysiology and management. Korean J Anesthesiol 2018;71(1):3-11.
4. Brooks DC, Schindler JL. Perioperative stroke: Risk assessment, prevention and treatment. Curr Treat Options Cardiovasc Med 2014;16(2):282.
5. Finelli PF. Diagnostic approach to restricted-diffusion patterns on MR imaging. Neurol Clin Pract 2012;2(4):287-93.
7. Nosan DK, Gomez CR, Maves MD. Perioperative stroke in patients undergoing head and neck surgery. Ann Otol Rhinol Laryngol 1993;102(9):717-23.
8. Cramer JD, Patel UA, Maas MB, Samant S, Smith SS. Is neck dissection associated with an increased risk of postoperative stroke? Otolaryngol Head Neck Surg 2017;157(2):226-32.
|
|
|||||||||||||||||||||||||||||||||||||||||||||

 |
 |